14.下列说法正确的是( )
| A. | 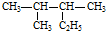 按系统命名法的名称为:2-甲基-3-乙基丁烷 按系统命名法的名称为:2-甲基-3-乙基丁烷 | |
| B. | 分子式为CH4O和C2H6O的物质一定互为同系物 | |
| C. | 根据纤维在火焰上燃烧产生的气味,可确定该纤维是否为蛋白纤维 | |
| D. | 等质量的甲醛、葡萄糖、纤维素完全燃烧时的耗氧量相等 |
13.下列说法正确的是( )
| A. | 用量筒量取10.00 mL 1.0mol•L-1的盐酸于100mL容量瓶中,加水定容至刻度,可配得0.1mol•L-1的盐酸 | |
| B. | 做焰色反应时,若连续做两个样品,应将铂丝用硫酸洗净并灼烧到无色 | |
| C. | 取试样与氢氧化钠浓溶液共热,产生能使湿润红色石蕊试纸变蓝色的气体,则说明试样中有NH4+ | |
| D. | 直接用分液的方法分离乙酸和乙酸乙酯 |
11.分子式为C5H10的有机物,该有机物能够使酸性高锰酸钾溶液褪色,该有机物可能的结构(不考虑顺反和空间结构)有多少种( )
| A. | 4种 | B. | 5种 | C. | 6种 | D. | 7种 |
10. 火箭发射常以液态肼(N2H4)为燃料,液态过氧化氢为助燃剂.
火箭发射常以液态肼(N2H4)为燃料,液态过氧化氢为助燃剂.
已知:N2H4(l)+O2(g)═N2(g)+2H2O(g)△H=-534kJ•mol-1
H2O2(l)═H2O(l)+$\frac{1}{2}$O2(g)△H=-98kJ•mol-1
H2O(l)═H2O(g)△H=44kJ•mol-1
(1)试写出N2H4和液态H2O2反应生成气态水的热化学方程式N2H4(l)+2H2O2(l)═N2(g)+4H2O(g)△H=-642kJ•mol-1.
(2)化学键的键能是指气态原子间形成1mol化学键时释放的能量.下表列出了某些
化学键的键能:
请回答下列问题:
①如图表示某反应的能量变化关系图,此反应为放热(填“放热”或“吸热”)反应,其中△H=(C-D)kJ•mol-1(用含C和D的字母表示);
②若此能量变化关系图表示如下反应:H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-241.8kJ•mol-1,则B=926kJ•mol-1,x=496.4.
 火箭发射常以液态肼(N2H4)为燃料,液态过氧化氢为助燃剂.
火箭发射常以液态肼(N2H4)为燃料,液态过氧化氢为助燃剂.已知:N2H4(l)+O2(g)═N2(g)+2H2O(g)△H=-534kJ•mol-1
H2O2(l)═H2O(l)+$\frac{1}{2}$O2(g)△H=-98kJ•mol-1
H2O(l)═H2O(g)△H=44kJ•mol-1
(1)试写出N2H4和液态H2O2反应生成气态水的热化学方程式N2H4(l)+2H2O2(l)═N2(g)+4H2O(g)△H=-642kJ•mol-1.
(2)化学键的键能是指气态原子间形成1mol化学键时释放的能量.下表列出了某些
化学键的键能:
| 化学键 | H-H | O=O | O-H |
| 键能 (kJ•mol-1) | 436 | x | 463 |
①如图表示某反应的能量变化关系图,此反应为放热(填“放热”或“吸热”)反应,其中△H=(C-D)kJ•mol-1(用含C和D的字母表示);
②若此能量变化关系图表示如下反应:H2(g)+$\frac{1}{2}$O2(g)═H2O(g)△H=-241.8kJ•mol-1,则B=926kJ•mol-1,x=496.4.
9.下列说法正确的是( )
| A. | 滴有碘水的淀粉溶液10ml分成两等份于两支试管,分别加入稀硫酸和唾液1ml,振荡,前者褪色快 | |
| B. | 恒温下,将盛有NO2和N2O4的平衡体系加压,体系颜色最终变浅 | |
| C. | 草酸溶液与酸性KMnO4溶液混合后,由于生成物对反应有催化作用,会使反应速率加快 | |
| D. | 在K2Cr2O7溶液中滴加浓硫酸,溶液颜色由橙色变黄色 |
8.某工厂的废液经测定其主要含有乙醇,此外还有丙酮、乙酸和乙酸乙酯.以上各物质的沸点如下:
现拟通过下列步骤回收乙醇和乙酸:
①向废液中加入甲溶液;②将混合液放入蒸馏器中缓缓加热;③收集温度在70℃~85℃之间的馏出物;④排出蒸馏器中的残液,冷却后向其中加入乙溶液(过量),然后再放入蒸馏器中进行蒸馏,收集馏出物.
可选用试剂:A.烧碱溶液 B.浓硫酸 C.饱和食盐水 D.浓盐酸
请回答下列问题:
(l)乙醇的沸点比丙酮沸点高的主要原因是乙醇分子之间易形成氢键.
(2)加入甲溶液是A,(填A B C D序号),涉及到的反应方程式:CH3COOCH2CH3+NaOH→CH3COONa+CH3CH2OH、CH3COOH+NaOH→CH3COONa+H2O.
(3)在70℃~85℃时馏出物的主要成分为乙醇.
(4)在步骤④中加入过量的乙溶液是B.(填A B C D序号),
(5)最后蒸馏的温度控制在117.9℃左右.
(6)在蒸馏操作中,仪器选择及安装都正确的是:(填标号)
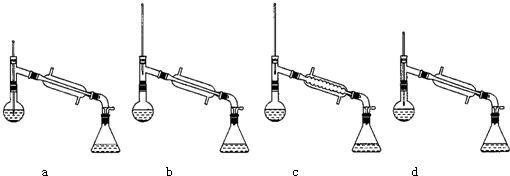
如果蒸馏前忘记加沸石,液体温度已接近沸点时,应该如何处理?b;移开热源,待温度降低,再投入沸石,重新加热.
| 物质 | 丙酮 | 乙酸乙酯 | 乙醇 | 乙酸 |
| 沸点/℃ | 56.2 | 77.06 | 78 | 117.9 |
①向废液中加入甲溶液;②将混合液放入蒸馏器中缓缓加热;③收集温度在70℃~85℃之间的馏出物;④排出蒸馏器中的残液,冷却后向其中加入乙溶液(过量),然后再放入蒸馏器中进行蒸馏,收集馏出物.
可选用试剂:A.烧碱溶液 B.浓硫酸 C.饱和食盐水 D.浓盐酸
请回答下列问题:
(l)乙醇的沸点比丙酮沸点高的主要原因是乙醇分子之间易形成氢键.
(2)加入甲溶液是A,(填A B C D序号),涉及到的反应方程式:CH3COOCH2CH3+NaOH→CH3COONa+CH3CH2OH、CH3COOH+NaOH→CH3COONa+H2O.
(3)在70℃~85℃时馏出物的主要成分为乙醇.
(4)在步骤④中加入过量的乙溶液是B.(填A B C D序号),
(5)最后蒸馏的温度控制在117.9℃左右.
(6)在蒸馏操作中,仪器选择及安装都正确的是:(填标号)

如果蒸馏前忘记加沸石,液体温度已接近沸点时,应该如何处理?b;移开热源,待温度降低,再投入沸石,重新加热.
7.下列说法中正确的是( )
| A. | 干冰汽化需吸收大量的热,这个变化是吸热反应 | |
| B. | 浓硫酸溶于水会放出大量热,这属于放热反应 | |
| C. | 用氢氧焰可以加热软化玻璃制玻璃器皿,这利用了氢气和氧气化合时放出的热量 | |
| D. | 木炭需加热到一定温度时才燃烧,所以木炭燃烧是吸热反应 |
6.下列有机物能与金属Na反应生成H2的是( )
0 152923 152931 152937 152941 152947 152949 152953 152959 152961 152967 152973 152977 152979 152983 152989 152991 152997 153001 153003 153007 153009 153013 153015 153017 153018 153019 153021 153022 153023 153025 153027 153031 153033 153037 153039 153043 153049 153051 153057 153061 153063 153067 153073 153079 153081 153087 153091 153093 153099 153103 153109 153117 203614
| A. | 乙醇 | B. | 苯酚 | C. | 氯苯 | D. | 乙醚 |
 如图是中学化学实验中出现频率较高的装置,它是由物质制备、生成物性质检验和尾气处理三部分组成.请你用中学化学常见试剂设计一个实验.通过乙中的反应和丙中的实验现象,得出三种物质性质递变的结论.试将试剂名称、丙中的实验现象及由此得出的实验结论填入下列空白处.
如图是中学化学实验中出现频率较高的装置,它是由物质制备、生成物性质检验和尾气处理三部分组成.请你用中学化学常见试剂设计一个实验.通过乙中的反应和丙中的实验现象,得出三种物质性质递变的结论.试将试剂名称、丙中的实验现象及由此得出的实验结论填入下列空白处.