题目内容
7.下列说法中正确的是( )| A. | 干冰汽化需吸收大量的热,这个变化是吸热反应 | |
| B. | 浓硫酸溶于水会放出大量热,这属于放热反应 | |
| C. | 用氢氧焰可以加热软化玻璃制玻璃器皿,这利用了氢气和氧气化合时放出的热量 | |
| D. | 木炭需加热到一定温度时才燃烧,所以木炭燃烧是吸热反应 |
分析 A.干冰汽化没有新的物质生成;
B.浓硫酸溶于水没有新的物质生成;
C.氢气和氧气化合时放出大量的热;
D.木炭燃烧时放出热量.
解答 解:A.干冰汽化是由固体直接变为气体,只是状态发生了改变,没有新的物质生成,属于物理变化,故A错误;
B.浓硫酸溶于水没有新的物质生成,属于物理变化,故B错误;
C.氢气和氧气化合时放出大量的热,用氢氧焰可以加热软化玻璃生产各种玻璃器皿,故C正确;
D.木炭需加热到一定温度达到木炭的着火点时才燃烧,木炭燃烧时放出热量,故D错误.
故选C.
点评 本题考查吸热和放热反应,难度不大,解答本题关键是要知道干冰升华属于物理变化,知道木炭燃烧都属于放热反应.

练习册系列答案
 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案
相关题目
17.将铜粉放入稀硫酸中,加热无明显现象发生,当加入下列一种物质后,铜粉的质量减小,溶液呈蓝色,同时有气体逸出,该物质是( )
| A. | Fe2(SO4)3 | B. | KNO3 | C. | Na2SO4 | D. | FeSO4 |
18.常温时,下列各组离子能大量共存的是( )
| A. | pH=1的无色溶液:Na+、Cu2+、NO3-、SO42- | |
| B. | 能溶解Al(OH)3固体的溶液:K+、Na+、HCO3-、SO42- | |
| C. | 水电离出的c(H+)=10-12mol/L的溶液:Ba2+、Na+、Cl-、NO3- | |
| D. | 能使淀粉KI试纸变蓝的溶液:K+、Fe2+、NO3-、Cl- |
15.下列有关化学与环境保护的说法正确的是( )
| A. | 就地在田间焚烧秸秆,减少运输成本 | |
| B. | 烧煤进行脱硫、脱硝处理,减少空气污染 | |
| C. | 推广和鼓励多使用私家车出行 | |
| D. | 做好空气质量预报工作,以使污染程度高是好预防 |
19.下列图示变化过程为吸热的是( )
| A. | 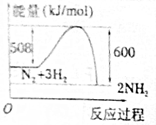 | B. | 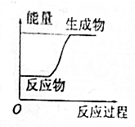 | ||
| C. | 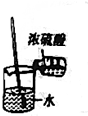 | D. | 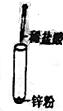 |
5.下列说法中,正确的是( )
| A. | 0.1mol/L醋酸钙溶液中,c (Ca 2+)>c(CH3COO-)>c(OH-)>c(H+) | |
| B. | 体积和pH 都相同的NH4Cl溶液、盐酸,完全溶解少量且等同的锌粉,前者用时少 | |
| C. | 将nmolH2(g)、nmol I2(g)和2nmolH2(g)、2nmolI2(g)分别充入两个恒温恒容的容器中,平衡时H2的转化率前者小于后者 | |
| D. | 某物质的溶液中由水电离出的c(H+)=1×10-amol/L,若a>7时,该溶液的pH一定为14-a |
6.下列说法正确的是( )
| A. | 常温下,将pH=2的HA溶液与pH=12的BOH溶液等体积混合后,溶液的pH<7,则BA为强酸弱碱盐 | |
| B. | 弱电解质溶液稀释后,溶液中各离子浓度一定都减小 | |
| C. | 常温下,向体积相同pH均为1的盐酸和醋酸溶液中分别加入足量锌片,两种溶液生成H2的体积相同 | |
| D. | 常温下,将pH均为13的NaOH溶液和氨水分别加水稀释100倍后,氨水的碱性强于NaOH溶液 |
