15.水溶液中的行为是中学化学的重要内容.
(1)25℃时,某溶液中由水电离出c(H+)=1×10-10 mol/L,该溶液pH为4或10.
(2)25℃时,测得亚硫酸氢钠溶液的pH<7,解释该溶液显酸性的原因(用离子方程式表示,并作适当解释)HSO3-+H2O?H2SO3+OH-HSO3-?H++SO32-,且电离程度大于水解程度,故溶液显酸性.
(3)电离常数是衡量弱电解质电离程度强弱的物理量.已知:
25℃时,将浓度相同的四种盐溶液:①NaCN ②NaClO ③Na2CO3 ④NaHCO3,按pH由大到小的顺序排列③>①>②>④(填序号),向84消毒液中通入少量的CO2,该反应的化学方程式为NaClO+CO2+H2O=NaHCO3+HClO.
(4)25℃时,将n mol•L-1的氨水与0.2mol•L-1的盐酸等体积混合,反应平衡时溶液中c(NH4+)=c(Cl-),则溶液显中性(填“酸”、“碱”或“中”),NH3•H2O的电离常数Kb=$\frac{2×1{0}^{-8}}{n-0.2}$(用含n的代数式表示).
(1)25℃时,某溶液中由水电离出c(H+)=1×10-10 mol/L,该溶液pH为4或10.
(2)25℃时,测得亚硫酸氢钠溶液的pH<7,解释该溶液显酸性的原因(用离子方程式表示,并作适当解释)HSO3-+H2O?H2SO3+OH-HSO3-?H++SO32-,且电离程度大于水解程度,故溶液显酸性.
(3)电离常数是衡量弱电解质电离程度强弱的物理量.已知:
| 化学式 | 电离常数(25℃) |
| HCN | K=4.9×10-10 |
| HClO | K=3×10-8 |
| H2CO3 | K1=4.3×10-7、K2=5.6×10-11 |
(4)25℃时,将n mol•L-1的氨水与0.2mol•L-1的盐酸等体积混合,反应平衡时溶液中c(NH4+)=c(Cl-),则溶液显中性(填“酸”、“碱”或“中”),NH3•H2O的电离常数Kb=$\frac{2×1{0}^{-8}}{n-0.2}$(用含n的代数式表示).
13. 在某容积一定的密闭容器中,有下列可逆反应:A(g)+B(g)?xC(g),有图Ⅰ所示的反应曲线,试判断对图Ⅱ的说法中正确的是(T表示温度,P表示压强,C%表示C的体积分数)( )
在某容积一定的密闭容器中,有下列可逆反应:A(g)+B(g)?xC(g),有图Ⅰ所示的反应曲线,试判断对图Ⅱ的说法中正确的是(T表示温度,P表示压强,C%表示C的体积分数)( )
 在某容积一定的密闭容器中,有下列可逆反应:A(g)+B(g)?xC(g),有图Ⅰ所示的反应曲线,试判断对图Ⅱ的说法中正确的是(T表示温度,P表示压强,C%表示C的体积分数)( )
在某容积一定的密闭容器中,有下列可逆反应:A(g)+B(g)?xC(g),有图Ⅰ所示的反应曲线,试判断对图Ⅱ的说法中正确的是(T表示温度,P表示压强,C%表示C的体积分数)( )| A. | P3<P4,y轴表示B的体积分数 | |
| B. | P3<P4,y轴表示混合气体的密度 | |
| C. | P3>P4,y轴表示B的百分含量 | |
| D. | P3>P4,y轴表示混合气体的平均摩尔质量 |
11.下面各容器中盛有海水,铁在其中被腐蚀时由快到慢的顺序是( )
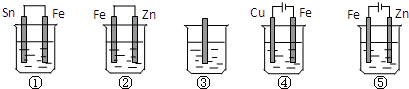

| A. | ①>②>③>④>⑤ | B. | ⑤>①>③>②>④ | C. | ⑤>①>②>③>④ | D. | ⑤>②>①>③>④ |
10.下列叙述正确的是( )
| A. |  和 和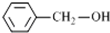 互为同系物 互为同系物 | |
| B. | 配制FeSO4溶液时,需加入少量铁粉和稀盐酸,既防止氧化又抑制水解 | |
| C. | 活化分子之间的碰撞不一定都是有效碰撞反应 | |
| D. | 对已建立化学平衡的某可逆反应,当改变条件使化学平衡向正反应方向移动时,生成物的百分含量一定增加 |
9.下列有机物实际存在且命名正确的是( )
0 152767 152775 152781 152785 152791 152793 152797 152803 152805 152811 152817 152821 152823 152827 152833 152835 152841 152845 152847 152851 152853 152857 152859 152861 152862 152863 152865 152866 152867 152869 152871 152875 152877 152881 152883 152887 152893 152895 152901 152905 152907 152911 152917 152923 152925 152931 152935 152937 152943 152947 152953 152961 203614
| A. | 2-甲基-5-乙基己烷 | B. | 3,3-二甲基-2-戊烯 | ||
| C. | 3-甲基-2-丁烯 | D. | 2,2-二甲基丙烷 |


 甲醇来源丰富、价格低廉、运输贮存方便,是一种重要的化工原料,有着重要的用途和应用前景.工业生产甲醇的常用方法是CO(g)+2H2(g)═CH3OH(g)△H<0.
甲醇来源丰富、价格低廉、运输贮存方便,是一种重要的化工原料,有着重要的用途和应用前景.工业生产甲醇的常用方法是CO(g)+2H2(g)═CH3OH(g)△H<0.