题目内容
16.现有五种溶液,分别含下列离子:①Ag+②Mg2+③Fe2+④Al3+⑤Fe3+.(1)写出符合下列条件的离子符号:
滴加氯水有明显现象的离子是Ag+ Fe2+,加铁粉后溶液增重的是Fe3+;
(2)向③的溶液中滴加NaOH溶液,现象是生成的白色絮状沉淀,迅速变成灰绿色,最后变成红褐色,反应过程中属于氧化还原反应的化学方程式4Fe(OH)2+2H2O+O2═4Fe(OH)3.
分析 (1)居于中间价态的离子既能被氧化又能被还原,滴加氯水溶液中氯气和水反应生成盐酸和次氯酸,氯气具有氧化性,银离子结合氯离子生成白色沉淀,亚铁离具有还原性,被氯气氧化铁离子,三价铁遇硫氰酸钾显红色,铁能将银从溶液中置换出来,能和三价铁化合为二价铁;
(2)亚铁离子和氢氧化钠反应生成的氢氧化亚铁沉淀很容易被氧气氧化为氢氧化铁.
解答 解:(1)Fe2+中Fe元素的化合价处于中间价态,既能被氧化又能被还原,滴加氯水溶液中氯气和水反应生成盐酸和次氯酸,氯气具有氧化性,银离子结合氯离子生成白色沉淀,Ag++Cl-=AgCl↓,亚铁离具有还原性,被氯气氧化铁离子,Cl2+2Fe2+=2Fe3++2Cl-,铁能与①⑤中的离子反应,对①溶中铁反应后析出了银,Fe+2Ag+=2Ag+Fe2+,溶液质量减轻,而铁能和三价铁反应生成二价铁,Fe+2Fe3+=3Fe2+,溶液质量增加了金属铁的质量,
故答案为:Ag+、Fe2+,Fe3+;
(2)亚铁离子和氢氧化钠反应生成的氢氧化亚铁沉淀很容易被氧气氧化为氢氧化铁,现象是:出现白色沉淀,迅速变为灰绿色最后变为红褐色,属于氧化还原反应的为4Fe(OH)2+O2+2H2O=4 Fe(OH)3,
故答案为:生成白色絮状沉淀,迅速变为灰绿色,最后变为红褐色沉淀;4Fe(OH)2+O2+2H2O=4Fe(OH)3.
点评 本题考查氧化还原反应,为高频考点,把握离子的性质、元素的化合价及氧化还原反应为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
相关题目
6.下列分子的立体构型和键角可用sp3杂化轨道来解释的是( )
①CH4 ②NH3 ③H2O ④CH≡CH ⑤苯 ⑥CH2=CH2.
①CH4 ②NH3 ③H2O ④CH≡CH ⑤苯 ⑥CH2=CH2.
| A. | ①②③ | B. | ①⑤⑥ | C. | ①②④ | D. | ③⑤⑥ |
7.下列实验操作或装置正确的是( )


| A. | 利用图1所示装置吸收制取少量二氧化硫产生的尾气 | |
| B. | 利用图2所示装置制取乙烯 | |
| C. | 利用图3所示装置证明H2CO3酸性强于苯酚 | |
| D. | 利用图4所示装置制备乙酸乙酯 |
11.下面各容器中盛有海水,铁在其中被腐蚀时由快到慢的顺序是( )
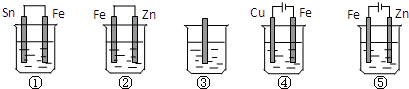

| A. | ①>②>③>④>⑤ | B. | ⑤>①>③>②>④ | C. | ⑤>①>②>③>④ | D. | ⑤>②>①>③>④ |
1.下列溶液中有关微粒的物质的量浓度关系正确的是( )
| A. | 物质的量浓度相等的①NH4HSO4溶液、②NH4HCO3溶液、③NH4Cl溶液中,pH的大小关系:②>①>③ | |
| B. | 常温下,将CH3COONa溶液和稀盐酸混合至溶液pH=7:c(Na+)>c(CH3COO-)>c(Cl-)=c(CH3COOH)>c(H+)=c(OH-) | |
| C. | 将lmolNaClO和2molNaHC03配制成1L混合溶液:c(HClO)+c(ClO-)=2c(HClO3-)+2c(H2CO3)+2c(CO32-) | |
| D. | 浓度均为0.1mol/L的NH3•H2O和NH4Cl溶液等体积混合后,若溶液呈碱性,则溶液中:C(NH4+)>c(Cl-)>c(NH3•H2O)>c(OH-)>c(H+) |
8.ClO2是一种消毒杀菌效率高、二次污染小的水处理剂.实验室可通过以下反应制得ClO2:2KClO3+H2C2O4+H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$2ClO2↑+K2SO4+2CO2↑+2H2O.下列说法正确的是( )
| A. | KClO3在反应中得到电子,发生氧化反应 | |
| B. | ClO2是氧化产物 | |
| C. | H2C2O4中+3价的碳元素在反应中被氧化 | |
| D. | 1mol KClO3参加反应有2 mol电子转移 |
8.下列实验操作中:①过滤②蒸发结晶③溶解④取液体试剂⑤取固体试剂⑥配制一定物质的量浓度的溶液.一定要用到玻璃棒的是( )
| A. | ①②③⑥ | B. | ④⑤ | C. | ①④⑥ | D. | ①③⑤⑥ |
9.某无色溶液中存在大量的H+、NH4+、Cl-,该溶液中还可能大量存在的离子是( )
| A. | K+ | B. | Ag+ | C. | OH- | D. | HCO3- |