15.卤族元素的单质和化合物很多,我们可以利用所学物质结构与性质的相关知识去认识和理解它们.
(1)卤族元素位于元素周期表的p区; 溴的价电子排布式为4s24p5.
(2)在一定浓度的溶液中,氢氟酸是以二分子缔合(HF) 2 形式存在的.使氢氟酸分子缔合的作用力是氢键.
(3)请根据下表提供的第一电离能数据判断,最有可能生成较稳定的单核阳离子的卤素原子是
碘(填名称).
(4)已知碘酸(HIO3)和高碘酸(H5IO6)的结构分别如图I、II 所示:
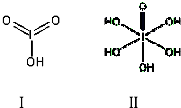
请比较二者酸性强弱:HIO3> H5IO6(填“>”、“<”或“=”).
(5)试分析 ClO2-中心氯原子的杂化类型sp3,试写出一个 ClO3-的等电子体Cl2O或OF2.
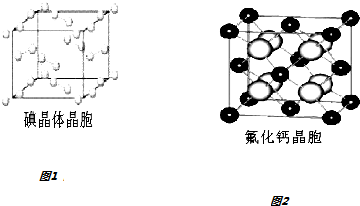
(6)图1为碘晶体晶胞结构.有关说法中正确的是AD.
A.碘分子的排列有2种不同的取向,2种取向不同的碘分子以4配位数交替配位形成层结构
B.用均摊法可知平均每个晶胞中有4个碘原子
C.碘晶体为无限延伸的空间结构,是原子晶体
D.碘晶体中存在的相互作用有非极性键和范德华力
(7)已知CaF2晶体(见图2)的密度为ρg/cm3,NA为阿伏加德罗常数,棱上相邻的两个Ca2+的核间距为a cm,则CaF2的相对分子质量可以表示为$\frac{a{\;}^{3}ρN{\;}_{A}}{4}$.
(1)卤族元素位于元素周期表的p区; 溴的价电子排布式为4s24p5.
(2)在一定浓度的溶液中,氢氟酸是以二分子缔合(HF) 2 形式存在的.使氢氟酸分子缔合的作用力是氢键.
(3)请根据下表提供的第一电离能数据判断,最有可能生成较稳定的单核阳离子的卤素原子是
碘(填名称).
| 氟 | 氯 | 溴 | 碘 | |
| 第一电离能(kJ/mol) | 1681 | 1251 | 1140 | 1008 |

请比较二者酸性强弱:HIO3> H5IO6(填“>”、“<”或“=”).
(5)试分析 ClO2-中心氯原子的杂化类型sp3,试写出一个 ClO3-的等电子体Cl2O或OF2.
(6)图1为碘晶体晶胞结构.有关说法中正确的是AD.
A.碘分子的排列有2种不同的取向,2种取向不同的碘分子以4配位数交替配位形成层结构
B.用均摊法可知平均每个晶胞中有4个碘原子
C.碘晶体为无限延伸的空间结构,是原子晶体
D.碘晶体中存在的相互作用有非极性键和范德华力
(7)已知CaF2晶体(见图2)的密度为ρg/cm3,NA为阿伏加德罗常数,棱上相邻的两个Ca2+的核间距为a cm,则CaF2的相对分子质量可以表示为$\frac{a{\;}^{3}ρN{\;}_{A}}{4}$.

13.在一个容积固定为2L的密闭容器中,发生反应:aA(g)+bB(g)?pC(g)△H=?,反应情况记录如表:
请根据表中数据仔细分析,回答下列问题:
(1)第2min到第4min内A的平均反应速率v(A)=0.1mol•L-1•min-1
(2)由表中数据可知反应在第4min到第6min时处于平衡状态,若在第2min、6min时分别改变了某一个反应条件,则改变的条件分别可能是:①第 2min使用催化剂、升高温度;②第 6min增加B的浓度;
(3)反应在第4min建立平衡,此温度下该反应的化学平衡常数 K=2.22.
(4)判断第9min时否(是/否)达平衡,说明理由因为Qc<K.
| 时间(min) | n(A)(mol) | n(B)(mol) | n(C)(mol) |
| 0 | 1 | 3 | 0 |
| 第2min | 0.8 | 2.6 | 0.4 |
| 第4min | 0.4 | 1.8 | 1.2 |
| 第6min | 0.4 | 1.8 | 1.2 |
| 第8min | 0.1 | 2.0 | 1.8 |
| 第9min | 0.05 | 1.9 | 0.3 |
(1)第2min到第4min内A的平均反应速率v(A)=0.1mol•L-1•min-1
(2)由表中数据可知反应在第4min到第6min时处于平衡状态,若在第2min、6min时分别改变了某一个反应条件,则改变的条件分别可能是:①第 2min使用催化剂、升高温度;②第 6min增加B的浓度;
(3)反应在第4min建立平衡,此温度下该反应的化学平衡常数 K=2.22.
(4)判断第9min时否(是/否)达平衡,说明理由因为Qc<K.
11.下列实验设计及其对应的离子方程式均正确的是( )
0 152674 152682 152688 152692 152698 152700 152704 152710 152712 152718 152724 152728 152730 152734 152740 152742 152748 152752 152754 152758 152760 152764 152766 152768 152769 152770 152772 152773 152774 152776 152778 152782 152784 152788 152790 152794 152800 152802 152808 152812 152814 152818 152824 152830 152832 152838 152842 152844 152850 152854 152860 152868 203614
| A. | 用FeCl3溶液腐蚀铜线路板:Cu+Fe3+═Cu2++Fe2+ | |
| B. | Na2O2与H2O反应制备O2:2Na2O2+2H2O═4Na++4OH-+O2↑ | |
| C. | 将氯气溶于水制备次氯酸:Cl2+H2O═2H++Cl-+ClO- | |
| D. | 用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO4-+6H++5H2O2═2Mn2++5O2↑+8H2O |

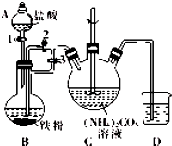 乳酸亚铁{[CH3CH(OH)COO]2Fe}广泛应用于乳制品、营养液等,能溶于水,可由乳酸与FeCO3反应制得.
乳酸亚铁{[CH3CH(OH)COO]2Fe}广泛应用于乳制品、营养液等,能溶于水,可由乳酸与FeCO3反应制得.