18.Ni(s)+4CO(g)?Ni(CO)4(g)在一密闭容器中,放入棉粉并充入一定量的CO气体,已知该反应平衡常数与温度的关系下表:下列说法正确的是( )
| 温度℃ | 25 | 80 | 230 |
| 平衡常数 | 5×104 | 2 | 1.9×10-5 |
| A. | 上述反应是熵增反应 | |
| B. | 在80℃时,测得某时刻Ni(CO)4、CO浓度均为0.5 mol•L-1,则此时反应逆向进行 | |
| C. | 25℃时,反应Ni(CO)4(g)?Ni(s)+4CO(g)的平衡常数是0.5 | |
| D. | 恒温恒容,向已达平衡的容器中再充入少量Ni(CO)4(g),达到新平衡时,CO的体积百分含量将减小 |
17.化合物Ⅲ是合成中药黄芩中的主要活性成分的中间体,合成方法如下:下列有关叙述正确的是( )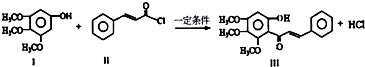

| A. | Ⅰ在空气中不能稳定存在 | |
| B. | 可用FeCl3溶液鉴别有机物Ⅱ和Ⅲ | |
| C. | Ⅱ中所有原子一定不可能共面 | |
| D. | 1mol产物Ⅲ与足量溴水反应,消耗Br2 的物质的量为1.5mol |
16.下列各组离子能够大量共存的是( )
| A. | Na+、Ca2+、Cl-、NO3- | B. | Fe2+、H+、SO32-、ClO- | ||
| C. | Mg2+、NH4+、Cl-、SO42- | D. | K+、Fe3+、NO3-、SCN- |
15.常温下,有体积相同的四种溶液:①pH=3的CH3COOH溶液;②pH=3的盐酸;③pH=11的氨水;④pH=11的NaOH溶液.下列说法正确的是( )
| A. | ④和②混合溶液中:c(H+)=c(OH-) | |
| B. | ①与④混合溶液中:c(Na+)=c(CH3COO-)+c(CH3COOH) | |
| C. | ②和③混合溶液中:c(H+)>c(OH-) | |
| D. | 四种溶液稀释100倍,溶液pH:③>④>②>① |
14.已知反应2SO2(g)+O2(g)?2SO3(g)△H=-198kJ•mol-1,向某体积恒定的密闭容器中充入1mol SO2和0.5molO2,在一定条件下发生反应,下图是某物理量(Y)随时间(t)变化的示意图,下列说法正确的是( )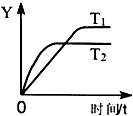

| A. | 温度T2<T1 | |
| B. | 反应达到平衡后放出99kJ的热量 | |
| C. | Y可能是SO2的转化率或SO3的浓度 | |
| D. | 反应达到平衡后容器内气体的密度减小 |
13.某pH=1的ZnCl2和HCl的混合溶液中含有FeCl3杂质,通过水解除去杂质,需将溶液调至pH=4,在调节溶液pH时,应选用的试剂是( )
| A. | NaO | B. | ZnO | C. | Na2CO3 | D. | Fe2O3 |
12.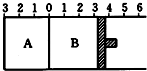 如图所示,温度不变下某容器分隔AB两部分,A容积固定不变,B有可移动的活塞,现在A中充入2molSO2和1molO2,在B中充入2mol SO3和1molN2,开始时活塞停在3处.在相同条件下发生可逆反应:2SO3(g)?2SO2(g)+O2(g),则下列说法正确的是( )
如图所示,温度不变下某容器分隔AB两部分,A容积固定不变,B有可移动的活塞,现在A中充入2molSO2和1molO2,在B中充入2mol SO3和1molN2,开始时活塞停在3处.在相同条件下发生可逆反应:2SO3(g)?2SO2(g)+O2(g),则下列说法正确的是( )
 如图所示,温度不变下某容器分隔AB两部分,A容积固定不变,B有可移动的活塞,现在A中充入2molSO2和1molO2,在B中充入2mol SO3和1molN2,开始时活塞停在3处.在相同条件下发生可逆反应:2SO3(g)?2SO2(g)+O2(g),则下列说法正确的是( )
如图所示,温度不变下某容器分隔AB两部分,A容积固定不变,B有可移动的活塞,现在A中充入2molSO2和1molO2,在B中充入2mol SO3和1molN2,开始时活塞停在3处.在相同条件下发生可逆反应:2SO3(g)?2SO2(g)+O2(g),则下列说法正确的是( )| A. | A中的压强大于B中的压强 | |
| B. | A中的SO2浓度小于B中SO2浓度 | |
| C. | A中的SO3浓度小于B中SO3浓度 | |
| D. | 将A改为可移动的活塞,达平衡时,A 停在0左侧0.5 处,则B可能停在0右侧3.2处 |
10.CO(g)+Cl2(g)?COCl2(g)△H<0,当反应达到平衡时,下列措施:①升温、②加压、③增加Cl2的浓度④加催化剂⑤恒压通入惰性气体⑥恒容通入惰性气体.能提高CO转化率的是( )
0 152559 152567 152573 152577 152583 152585 152589 152595 152597 152603 152609 152613 152615 152619 152625 152627 152633 152637 152639 152643 152645 152649 152651 152653 152654 152655 152657 152658 152659 152661 152663 152667 152669 152673 152675 152679 152685 152687 152693 152697 152699 152703 152709 152715 152717 152723 152727 152729 152735 152739 152745 152753 203614
| A. | ②③ | B. | ③⑤ | C. | ①④ | D. | ③⑥ |
 ;
; ;
; .
.