11.下列反应对应的离子方程式书写正确的是( )
| A. | 氢氧化钠溶液与稀硫酸的反应:2OH-+2H+═2H2O | |
| B. | 硫酸铜溶液中滴加氢氧化钡溶液:Ba2++2OH-+Cu2++SO42-═BaSO4↓+Cu(OH)2↓ | |
| C. | 硝酸银溶液中加入铜粉:Cu+Ag+═Cu2++Ag | |
| D. | 向盐酸中投入碳酸钙:CO32-+2H+═H2O+CO2↑ |
10.500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为( )
| A. | N2(g)+3H2(g)$?_{500℃、30MPa}^{催化剂}$2MH3(g)△H=-38.6kJ•mol-1 | |
| B. | N2(g)+3H2(g)═2NH3(g)△H=-38.6kJ•mol-1 | |
| C. | N2(g)+3H2(g)═2NH3(g)△H=38.6kJ•mol-1 | |
| D. | 不能确定 |
9.下列说法正确的是( )
| A. | 治疗胃酸过多,可用NaHCO3,不能用Al(OH)3,因其含有Al元素 | |
| B. | Al箔用砂纸打磨后,在空气中受热可以熔化,由于氧化膜被破坏,熔化的Al可以滴落 | |
| C. | 用铂丝做焰色反应实验,每次做完后都需要用盐酸洗涤,再灼烧至跟酒精灯火焰颜色相同后再使用 | |
| D. | 实验室制备Al(OH)3时,氨水不宜过量,因为Al(OH)3与过量的浓氨水反应生成NH4AlO2 |
8.向硫酸铜溶液中加入一小块金属钠后,观察到的现象有( )
①钠浮于液面上 ②熔化成小球 ③发出嘶嘶的响声,放出气体 ④有蓝色沉淀产生 ⑤钠周围蓝色沉淀部分变黑 ⑥析出大量红色的铜 ⑦小球沉在溶液底部 ⑧小球在液面上游动、逐渐变小,直至消失.
①钠浮于液面上 ②熔化成小球 ③发出嘶嘶的响声,放出气体 ④有蓝色沉淀产生 ⑤钠周围蓝色沉淀部分变黑 ⑥析出大量红色的铜 ⑦小球沉在溶液底部 ⑧小球在液面上游动、逐渐变小,直至消失.
| A. | ①②③④⑤⑥ | B. | ①②③④⑤⑧ | C. | ①②③⑥⑧ | D. | ②⑥⑦ |
6.某实验室制取苯甲酸的过程如下:
(一)如图所示,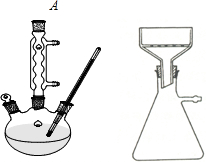
向250mL三颈瓶中加入2.7mL(2.3g)甲苯和100mL水,瓶口装仪器A,加热至沸.从仪器A上口分批加入8.5g高锰酸钾.用少量水(约25mL)将粘在仪器A内壁的高锰酸钾冲洗入烧瓶内.继续煮沸并间歇摇动烧瓶直到甲苯层消失,回流液不再有明显油珠,反应如下:

(二)将反应混合物趁热过滤,用少量热水洗涤滤渣二氧化锰,用玻棒小心搅动(不要使滤纸松动).滤液并倒入400mL烧怀中,将烧杯冷却,然后用浓盐酸酸化,直到苯甲酸全部析出为止;得纯净的苯甲酸质量为1.83g.苯甲酸在不同温度下的溶解度如表:
(1)仪器A的名称是球形冷凝管,(1分)冷却水的进出口方向低进高出
(2)加热前,应先向三颈瓶中加入沸石,其目的是防止暴沸.
(3)反应结束时,溶液还显紫红色,可通过三颈瓶的一个口,向其中加入Na2SO3溶液,发生反应的离子方程式是2MnO4-+3SO32-+H2O=2MnO2+3SO42-+2OH-.(提示:在本实验条件下,高锰酸钾的还原产物是MnO2)
(4)烧杯中的滤液要快速充分冷却,冷却时应将烧杯应放在冷水浴中冷却;然后用浓盐酸酸化,目的是: (用化学方程式表示).
(用化学方程式表示).
(一)如图所示,

向250mL三颈瓶中加入2.7mL(2.3g)甲苯和100mL水,瓶口装仪器A,加热至沸.从仪器A上口分批加入8.5g高锰酸钾.用少量水(约25mL)将粘在仪器A内壁的高锰酸钾冲洗入烧瓶内.继续煮沸并间歇摇动烧瓶直到甲苯层消失,回流液不再有明显油珠,反应如下:

(二)将反应混合物趁热过滤,用少量热水洗涤滤渣二氧化锰,用玻棒小心搅动(不要使滤纸松动).滤液并倒入400mL烧怀中,将烧杯冷却,然后用浓盐酸酸化,直到苯甲酸全部析出为止;得纯净的苯甲酸质量为1.83g.苯甲酸在不同温度下的溶解度如表:
| 温度/℃ | 4 | 18 | 75 |
| 溶解度/[g•(100gH2O)-1] | 0.18 | 0.27 | 2.2 |
(2)加热前,应先向三颈瓶中加入沸石,其目的是防止暴沸.
(3)反应结束时,溶液还显紫红色,可通过三颈瓶的一个口,向其中加入Na2SO3溶液,发生反应的离子方程式是2MnO4-+3SO32-+H2O=2MnO2+3SO42-+2OH-.(提示:在本实验条件下,高锰酸钾的还原产物是MnO2)
(4)烧杯中的滤液要快速充分冷却,冷却时应将烧杯应放在冷水浴中冷却;然后用浓盐酸酸化,目的是:
 (用化学方程式表示).
(用化学方程式表示).
4.下列有关实验操作说法中,不正确的是( )
| A. | 向25mL沸水中滴加5-6滴稀的FeCl3溶液制备氢氧化铁胶体 | |
| B. | 用量筒、试管、胶头滴管、玻璃棒、蒸馏水和 pH试纸,可鉴别pH 相等的硫酸和醋酸 | |
| C. | 用FeSO4、NaOH和盐酸等试剂在空气中可以制备纯净的FeCl3溶液 | |
| D. | 用NaOH溶液和盐酸可除去MgCl2溶液中混有的AlCl3 |
3.使用石油热裂解的副产物CH4来制取CO和H2,其生产流程如图1:

此流程的第Ⅰ步反应为:CH4+H2O?CO+3H2,一定条件下CH4的平衡转化率与温度、压强的关系如图2.则P1<P2.100℃时,将1mol CH4和2mol H2O通入容积为100L的恒容密闭容器中,达到平衡时CH4的转化率为0.5.此时该反应的平衡常数K=2.25×10-4(.
此流程的第Ⅱ步反应的平衡常数随温度的变化如表:
从表中可以推断:该反应是放热反应,若在500℃时进行,设起始时CO和H2O的起始浓度均为0.020mol/L,在该条件下,反应达到平衡时,CO的转化率为75%.如图3表示该反应在t1时刻达到平衡、在t2时刻因改变某个条件引起浓度变化的情况:图中t2时刻发生改变的条件是降低温度,或增加水蒸汽的量,或减少氢气的量.
工业上常利用反应Ⅰ产生的CO和H2合成可再生能源甲醇.
①已知CO、CH3OH的燃烧热分别为283.0kJ•mol-1和726.5kJ•mol-1,则CH3OH不完全燃烧生成CO和H2O的热化学方程式为CH3OH(l)+O2(g)=CO(g)+2 H2O(l)△H=-443.5kJ•mol-1.
②合成甲醇的方程式为:CO+2H2?CH3OH△H<0.在230°C〜270℃最为有利.为研究合成气最合适的起始组成比n:n,分别在230℃、250℃和270℃进行实验,结果如图4所示.其中270℃的实验结果所对应的曲线是Z;当曲线X、Y、Z对应的投料比达到相同的CO平衡转化率时,对应的反应温度与投较比的关系是投料比越高,对应的反应温度越高.
③当投料比为1:1,温度为230℃,平衡混合气体中,CH3OH的物质的量分数为33.3%.

此流程的第Ⅰ步反应为:CH4+H2O?CO+3H2,一定条件下CH4的平衡转化率与温度、压强的关系如图2.则P1<P2.100℃时,将1mol CH4和2mol H2O通入容积为100L的恒容密闭容器中,达到平衡时CH4的转化率为0.5.此时该反应的平衡常数K=2.25×10-4(.
此流程的第Ⅱ步反应的平衡常数随温度的变化如表:
| 温度/℃ | 400 | 500 | 830 |
| 平衡常数K | 10 | 9 | 1 |
工业上常利用反应Ⅰ产生的CO和H2合成可再生能源甲醇.
①已知CO、CH3OH的燃烧热分别为283.0kJ•mol-1和726.5kJ•mol-1,则CH3OH不完全燃烧生成CO和H2O的热化学方程式为CH3OH(l)+O2(g)=CO(g)+2 H2O(l)△H=-443.5kJ•mol-1.
②合成甲醇的方程式为:CO+2H2?CH3OH△H<0.在230°C〜270℃最为有利.为研究合成气最合适的起始组成比n:n,分别在230℃、250℃和270℃进行实验,结果如图4所示.其中270℃的实验结果所对应的曲线是Z;当曲线X、Y、Z对应的投料比达到相同的CO平衡转化率时,对应的反应温度与投较比的关系是投料比越高,对应的反应温度越高.
③当投料比为1:1,温度为230℃,平衡混合气体中,CH3OH的物质的量分数为33.3%.
2.下列各说法中,正确的是( )
0 151838 151846 151852 151856 151862 151864 151868 151874 151876 151882 151888 151892 151894 151898 151904 151906 151912 151916 151918 151922 151924 151928 151930 151932 151933 151934 151936 151937 151938 151940 151942 151946 151948 151952 151954 151958 151964 151966 151972 151976 151978 151982 151988 151994 151996 152002 152006 152008 152014 152018 152024 152032 203614
| A. | △H>0表示放热反应,△H<0表示吸热反应 | |
| B. | 热化学方程式中的化学计量数只表示物质的量,可以是分数也可以是小数 | |
| C. | 1molH2SO4和1mo Ba(OH)2反应生成BaSO4沉淀时放出的热叫做中和热 | |
| D. | 1molH2和0.5mol O2反应放出的热就是H2的燃烧热 |
