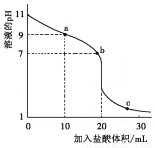
用4种溶液进行试验,下表中“操作及现象”与“溶液”对应关系错误的是 ( )
选项 | 操作及现象 | 溶液 |
A | 通入CO2,溶液变浑浊。再升温至65℃以上,溶液变澄清 | C6H5ONa溶液 |
B | 通入CO2,溶液变浑浊。继续通CO2至过量,浑浊消失 | NaSiO3溶液 |
C | 通入CO2,溶液变浑浊。再加入品红溶液,红色褪去 | Ca(ClO)2溶液 |
D | 通入SO2,溶液变浑浊。继续通SO2至过量,浑浊消失。再加入足量NaOH溶液,又变浑浊 | Ca(OH)2 |
乙醇是重要的有机化工原料,可由乙烯直接水合法或间接水合法生产。回答下列问题:
(1)间接水合法是指先将乙烯与浓硫酸反应生成硫酸氢乙酯(C2H5OSO3H)。再水解生成乙醇。写出相应的反应的化学方程式 。
(2)已知:乙烯气相直接水合反应如下:
C2H4(g)+H2O(g) 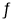 C2H5OH(g) H=-45.5KJ/mol
C2H5OH(g) H=-45.5KJ/mol
下图为气相直接水合法中乙烯的平衡转化率与温度、压强的关系(其中n(H2O):n(C2H4)=1:1)
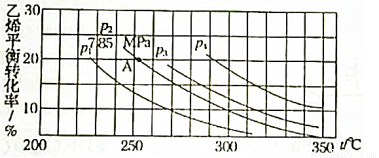
①计算乙烯水合制乙醇反应在图中A点的平衡常数Kp= (Kp表示用平衡分压代替平衡浓度计算出的平衡常数的值,分压=总压×物质的量分数)
②图中压强P1、P2、P3、P4的大小顺序为: ,理由是 。
(3)若某温度下,反应C2H4(g)+H2O(g) 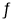 C2H5OH(g)的平衡常数为Kp=0.05MPa-1,体系总压为8.00MPa,各物质的量分数如下表所示。
C2H5OH(g)的平衡常数为Kp=0.05MPa-1,体系总压为8.00MPa,各物质的量分数如下表所示。
物质 | C2H4(g) | H2O(g) | C2H5OH(g) |
物质的量分数 | 0.25 | 0.25 | 0.5 |
则v(正) v(逆)(填“>”“<”“=”)。
现有常温下的四种溶液(如下表),下列有关叙述中正确的是
① | ② | ③ | ④ | |
溶液 | 氨水 | 氢氧化钠溶液 | 醋酸 | 盐酸 |
pH | 11 | 11 | 3 | 3 |
A.V1L④与V2L②溶液混合后,若混合后溶液pH=4,则V1:V2=9:11
B.在①、②中分别加入适量的氯化铵晶体后,①的pH减小,②的pH不变
C.分别加水稀释10倍、四种溶液的pH:①>②>③>④
D.将①、④两种溶液等体积混合,所得溶液中:c (NH4+)>c(Cl-)>c(OH-)>c(H+)
下表是某铬酸(H2CrO4)溶液中离子浓度(mol.L-1)与pH的关系,下列说法不正确的是
pH | c(CrO42-) | c(HCrO4-) | c( Cr2O72-)] | c(H2CrO4) |
4 | 0.0003 | 0.1040 | 0.4480 | 0 |
6 | 0.0319 | 0.0999 | 0.4370 | 0 |
7 | 0.2745 | 0.0860 | 0.3195 | 0 |
9 | 0.9960 | 0.0031 | 0.0004 | 0 |
A.铬酸的第一步电离是完全电离
B.铬酸的第二步电离是部分电离,且存在两种电离方式
C.当电离达到平衡时,2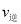 (Cr2O72-)=
(Cr2O72-)=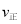 (HCrO4-)
(HCrO4-)
D.pH越大,电离出的CrO42-浓度越大

 HCO3-+OH-
HCO3-+OH-