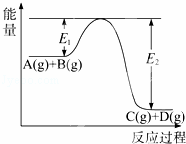
在100℃时,将0.100mol的N2O4气体充入1L抽空的密闭容器中,隔一定时间对该容器内的物质进行分析,得到如下表格:
| 时间/s 浓度mol•L﹣1 | 0 | 20 | 40 | 60 | 80 | 100 |
| c(N2O4)mol•L﹣1 | 0.100 | c1 | 0.050 | c3 | a | b |
| c(NO2)/mol•L﹣1 | 0.000 | 0.060 | c2 | 0.120 | 0.120 | 0.120 |
试填空:
(1)达到平衡时N2O4的转化率为 %.
(2)20s的四氧化二氮的浓度c1= mol•L﹣1,在0s~20s内四氧化二氮的平均反应速率为 mol•(L•s)﹣1;.
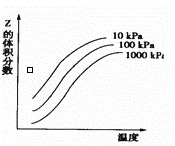
如图表示温度和压强对平衡X+Y⇌2Z的影响.下列叙述正确的是( )
|
| A. | 增大压强,平衡向右移动 |
|
| B. | 升高温度,平衡向左移动 |
|
| C. | X和Y中只有一种为气态,Z为气态 |
|
| D. | 上述反应的正反应为放热反应 |
在恒温恒容的密闭容器中,对于反应2SO2(g)+O2(g)⇌2SO3(g),下列说法正确的是( )
|
| A. | 增大O2的浓度,SO3的化学反应速率减慢 |
|
| B. | 1molSO2与过量的O2反应,一定生成1molSO3 |
|
| C. | 起始投入2molSO2、1molO2与起始投入2molSO3,达到平衡状态时,SO3的体积分数相等 |
|
| D. | 往平衡体系中充入一定量的N2,使体系的压强增大,平衡正向移动 |
一定温度下,向a L密闭容器中加入2mol NO2(g),发生如下反应:2NO2⇌2NO+O2,此反应达到平衡状态的标志是( )
|
| A. | 混合气体的密度不再变化 |
|
| B. | 混合气体的颜色变浅 |
|
| C. | 混合气体中NO2、NO、O2的物质的量之比为2:2:1 |
|
| D. | 单位时间内生成2n mol NO同时生成2n mol NO2 |
一定条件下,往容积恒定的密闭容器中投入2molA和1molB,发生可逆反应:2A(g)+B(g)⇌C(g)+D(s),达到平衡时,测得压强为原压强的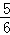 ,则A的转化率为( )
,则A的转化率为( )
|
| A. | 25% | B. | 40% | C. | 50% | D. | 75% |
对于可逆反应A(g)+B(g)⇌C(g)△H<0,下列图象正确的是( )
|
| A. |
| B. |
| C. |
| D. |
|
反应4A(g)+5B(g)═4C(g)+6D(g),在5L的密闭容器中进行,半分钟后,C的物质的量增加了0.30mol.下列叙述正确的是( )
|
| A. | A的平均反应速率是0.010 mol•L﹣1•s﹣1 |
|
| B. | 容器中含D物质的量至少为0.45 mol |
|
| C. | 容器中A、B、C、D的物质的量的比一定是4: 5:4:6 |
|
| D. | 容器中A的物质的量一定增加了0.30 mol |
下列各组物质的颜色变化,可用勒夏特列原理解释的是( )
|
| A. | 光照氯水,颜色变浅 |
|
| B. | 向盛有NO2的集气瓶中投入活性炭,颜色变浅 |
|
| C. | 加热氯化铁溶液,溶液变浑 |
|
| D. | 压缩H2与I2(g)反应的平衡混合气体,颜色变深 |
可以增加反应物分子中活化分子的百分数的是①反应反应的浓度 ②增大压强 ③升高温度 ④使用催化剂 ⑤减小压强 ⑥降低温度( )
|
| A. | ①②③④ | B. | ②③ | C. | ③④ | D. | 全部 |