下表为元素周期表的一部分,a、b、c…为部分元素.回答下列问题:
| a |
| ||||||||||||||||
| b | c | d | e |
| |||||||||||||
| f | g |
| |||||||||||||||
| h | i |
(1)请写出上述元素h的原子结构示意图 ;
(2)比较e、g两种元素的气态氢化物的稳定性大小 (写化学式,下同);e、g两种元素的气态氢化物熔、沸点较高的是 ,其原为 ;
(3)b2a2分子的电子式是 ,该分子中存在的σ键与π键的个数比为 ;
(4)c、d两种元素中第一电离能较大的是 (写元素符号),其原因是
;
(5)已知f的氢氧化物与水电离出的OH﹣可形成配位键,则生成的含有配位键的离子的结构式为 (标出配位键).
正硼酸(H3BO3)是一种片层状结构白色晶体,层内的H3BO3分子通过氢键相连(如图).下列有关说法正确的是( )

|
| A. | 正硼酸晶体中只存在氢键 |
|
| B. | H3BO3分子的稳定性与氢键无关 |
|
| C. | 分子中硼原子最外层为8e﹣稳定结构 |
|
| D. | 含1molH3BO3的晶体中有6mol氢键 |
下列变化或数据与氢键无关的是( )
|
| A. | 水凝结成冰时,密度变小 |
|
| B. | 氨分子与水分子形成一水合氨 |
|
| C. | 水在2000℃时,只有4%的H2O发生分解 |
|
| D. | SbH3的沸点比PH3高 |
科学家研究发现:等电子体的空间结构相同,则下列有关说法中正确的是( )
|
| A. | BF3和CO32﹣是等电子体,均为平面正三角形结构 |
|
| B. | B3N3H6和苯(C6H6)是等电子体,B3N3H6分子中不存在“肩并肩”式重叠的轨道 |
|
| C. | NH3和PCl3是等电子体,均为三角锥形结构 |
|
| D. | CH4和NH4+是等电子体,键角均为60° |
已知A、B、C均为短周期的元素,A、B同周期、A、C的最低价离子分别为A2﹣和C﹣,B2+和C﹣具有相同的电子层结构,下列说法正确的是( )
|
| A. | C元素的最高正价为+7价 |
|
| B. | 离子半径:A2﹣>C﹣>B2+ |
|
| C. | 对应气态氢化物的稳定性:A>C |
|
| D. | 还原性:A2﹣>C﹣ |
向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续添加氨水,难溶物溶解得到深蓝色的透明溶液.下列对此现象说法正确的是( )
|
| A. | 反应后溶液中不存在任何沉淀,所以反应前后Cu2+的浓度不变 |
|
| B. | 氢氧化铜可溶于氨水说明氢氧化铜是两性氢氧化物 |
|
| C. | 在[Cu(NH3)4]2+离子中,Cu2+提供空轨道,NH3给出孤电子对 |
|
| D. | 在[Cu(NH3)4]2+离子中,Cu2+给出孤电子对,NH3提供空轨道 |
肯定属于同族元素且性质相似的是( )
|
| A. | 原子核外电子排布式:A为1s22s2,B为1s2 |
|
| B. | 结构示意图:A为 |
|
| C. | A原子基态时2p轨道上有1个未成对电子,B原子基态时3p轨道上也有1个未成对电子 |
|
| D. | A原子基态时2p轨道上有一对成对电子,B原子基态时3p轨道上也有一对成对电子 |

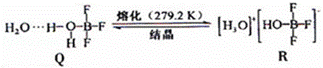
 ,B为
,B为