下列关于丙烯(CH3﹣CH=CH2)的说法正确的( )
|
| A. | 丙烯分子有8个σ键,1个π键 |
|
| B. | 丙烯分子中3个碳原子都是sp3杂化 |
|
| C. | 丙烯分子不存在非极性键 |
|
| D. | 丙烯分子中3个碳原子在同一直线 |
现有四种基态原子的电子排布式:①1s22s22p63s23p4,②1s22s22p63s23p3,③1s22s22p3,④1s22s22p5,下列比较中正确的是( )
|
| A. | 第一电离能:④>③>②>① | B. | 原子半径:④>③>②>① |
|
| C. | 电负性:④>③>①>② | D. | 最高正化合价:④>③=②>① |
下图为元素周期表前4周期的一部分,下列有关R、W、X、Y、Z 5种元素的叙述中,正确的是( )
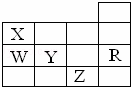
|
| A. | W、R元素单质分子内的都存在非极性键 |
|
| B. | X、Z元素都能形成双原子分子 |
|
| C. | 键能W﹣H<Y﹣H,键的极性Y﹣H>W﹣H |
|
| D. | 键长X﹣H<W﹣H,键能X﹣H<W﹣H |
设NA为阿伏伽德罗常数,下列说法中正确的是( )
|
| A. | 7.8g过氧化钠固体中含阴离子个数为0.2NA |
|
| B. | 34g氨气中含N﹣H的数目为6NA |
|
| C. | 标准状况下,22.4L乙炔中含π键数为2NA |
|
| D. | 1molNaHSO4晶体中阳离子数为2NA |
两种微粒含有相同的质子数和电子数,这两种微微粒可能是( )
①两种不同的原子;
②两种不同元素的原子;
③一种原子和一种分子;
④一种原子和一种离子;
⑤两种不同分子;
⑥一种分子和一种离子;
⑦两种不同阳离子;
⑧两种不同阴离子.
|
| A. | ①③⑤⑥⑦⑧ | B. | ①③⑤⑦⑧ | C. | ①③④⑤⑦ | D. | 全部都是 |
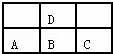
如图是元素周期表短周期的一部分,若A原子最外层的电子数比次外层的电子数少3,则下列说法中正确的是( )
|
| A. | D与C不能形成化合物 |
|
| B. | D的最高正价与B的最高正价相等 |
|
| C. | A、B、C的最高价氧化物对应的水化物酸性强弱的关系是C>B>A |
|
| D. | A、B、C、D原子所具有的原子轨道类型和数目都相同 |
下列反应中,既有共价键的断裂,又有离子键的形成的是( )
|
| A. | 盐酸和氢氧化钠溶液反应 |
|
| B. | 氯化氢气体溶解于水 |
|
| C. | 氯化氢气体遇到氨气产生“白烟” |
|
| D. | 锌片投入稀硫酸中产生气体 |
下列各组中,元素的电负性递增的是( )
|
| A. | Na K Rb | B. | N B Be | C. | O S Se | D. | Na P N |
下列叙述中正确的是( )
|
| A. | 在离子化合物中不可能存在非极性键 |
|
| B. | 气体单质分子中一定存在非极性键 |
|
| C. | 在共价化合物中不可能存在离子键 |
|
| D. | 由非金属元素组成的化合物一定是共价化合物 |
下列分子中所有原子都满足最外层8电子结构的是( )
|
| A. | COCl2 | B. | XeF2 | C. | BF3 | D. | SF6 |