对于处于化学平衡状态的反应C(s)+H2O(g)⇌CO(g)+H2(g)△H>0,既要提高反应速率又要提高H2O的转化率,下列措施中可行的是( )
|
| A. | 增大H2O(g)的浓度 | B. | 降低压强 |
|
| C. | 升温 | D. | 使用合适的催化剂 |
在一定条件下,能说明可逆反应X(g)+Y(g)⇌Z(g)+W(g)已经达到平衡状态的是( )
|
| A. | 容器内压强不随时间的变化而变化 |
|
| B. | X、Y、Z、W的浓度比保持不变 |
|
| C. | X的消耗速率与Z的生成速率相等 |
|
| D. | c(X)•c(Y)=c(Z)•c(W) |
化学平衡主要研究下列哪一类反应的规律( )
|
| A. | 可逆反应 | B. | 化合反应 | C. | 离子反应 | D. | 气体反应 |
铁的锈蚀是工业上研究的重点内容.为研究铁锈蚀的影响因素,某同学用相同的铁丝在不同的气流中做了如下探究实验,记录如下:
| 序号 | 铁丝状态 | 温度℃ | 气流湿度 | 气流成分 | 时间 | 现象 |
| ① | 洁净光亮 | 25 | 干燥 | 空气 | 一个月 | 铁丝表面光亮 |
| ② | 洁净光亮 | 25 | 潮湿 | 空气 | 一天 | 铁丝表面光亮 |
| ③ | 洁净光亮 | 25 | 潮湿 | 空气 | 一个月 | 铁丝表面已经变暗 |
| ④ | 洁净光亮 | 25 | 潮湿 | 氧气 | 一天 | 铁丝表面略微变暗 |
| ⑤ | 洁净光亮 | 40 | 潮湿 | 氧气 | 一天 | A |
| ⑥ | 光亮铁丝表面有氯化钠溶液 | 25 | 潮湿 | 氧气 | 一天 | 铁丝表面变暗程度比④严重 |
回答以下问题:
(1)上述实验中发生了吸氧腐蚀的是 (填实验序号),正极反应式是 ﹣
(2)实验④⑥说明 是影响铁锈蚀的主要因素.如果实验④⑤是为说明温度对铁锈蚀速率的影响,则A处观察到的现象可能是 .
(3)为防止铁的锈蚀,地下埋的水管采用外接电源阴极保护法,则水管接电源的 极(填“正”或“负”)
Ⅰ.如图1为向25mL 0.1mol•L﹣1NaOH溶液中逐滴滴加0.2mol•L﹣1CH3COOH溶液过程中溶液pH的变化曲线.请回答:
(1)B点溶液呈中性,有人据此认为,在B点时NaOH与CH3COOH恰好完全反应,这种看法是否正确? (选填“是”或“否”).若不正确,则二者恰好完全反应的点是在AB区间还是BD区间内? 区间(若正确,此问不答).
(2)关于该滴定实验,从下列选项中选出最恰当的一项 (选填字母).
| 锥形瓶中溶液 | 滴定管中溶液 | 选用指示剂 | 选用滴定管 | |
| A | 碱 | 酸 | 酚酞 | (乙) |
| B | 酸 | 碱 | 甲基橙 | (甲) |
| C | 碱 | 酸 | 石蕊 | (甲) |
| D | 酸 | 碱 | 酚酞 | (乙) |
(3)AB区间,c(OH﹣)>c(H+),则c(OH﹣)与c(CH3COO﹣)大小关系是 .
A.c(OH﹣)大于c(CH3COO﹣) B.c(OH﹣)小于c(CH3COO﹣)
C.c(OH﹣)等于c(CH3COO﹣) D.上述三种情况都可以
(4)在D点时,溶液中c(CH3COO﹣)+c(CH3COOH) 2c(Na+)(填“>”“<”或“=”).
Ⅱ.t℃时,某稀硫酸溶液中c(H+)=10﹣amol•L﹣1,c(OH﹣)=10﹣bmol•L﹣1,已知a+b=13:
(5)该温度下水的离子积常数Kw的数值为 .
(6)该温度下(t℃),将100mL 0.1mol•L﹣1的稀H2SO4与100mL 0.4mol•L﹣1的NaOH溶液混合(溶液体积变化忽略不计),溶液的pH= .
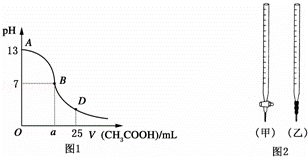

 ,上述条件下,溶液②中的
,上述条件下,溶液②中的 浓度为
浓度为