下列各项中操作或现象能达到预期实验目的的是 ( )
| 选项 | 实验目的 | 操作或现象 |
| A | 检验碳与浓硫酸反应后的气体产物 | 将产生的气体依次通过无水CuSO4、澄清石灰水和品红溶液 |
| B | 证明蛋白质在某些无机盐溶液作用下发生变性 | 向鸡蛋清溶液中加入饱和硫酸钠溶液,有沉淀析出;再把沉淀加入蒸馏水中 |
| C | 检验溴乙烷中的溴元素 | 将少量溴乙烷与NaOH溶液混合共热,充分反应并冷却后,向溶液中加稀HNO3酸化,再滴加AgNO3溶液 |
| D | 证明溶液中存在平衡: Fe3++3SCN-Fe(SCN)3 | 将1 mL KSCN溶液与1 mL同浓度FeCl3溶液充分混合;再继续加入KSCN溶液,溶液颜色加深 |
 。
。  6Cu+SO2↑,该反应的氧化剂是 ;当生成19.2 g Cu时,反应中转移的电子为 mol。
6Cu+SO2↑,该反应的氧化剂是 ;当生成19.2 g Cu时,反应中转移的电子为 mol。  学方程式为I2+2Na2S2O3
学方程式为I2+2Na2S2O3 2NaI+Na2S4O6,平均消耗c
2NaI+Na2S4O6,平均消耗c Na
Na 2S2O3
2S2O3

 备铝时,需加入冰晶石(Na3AlF6),其作
备铝时,需加入冰晶石(Na3AlF6),其作 用是 ,工业上可以用氟化氢气体、氢氧化铝和纯碱在高温条件下发生反应来制取冰晶石,写出该反应的化学方程式: 。
用是 ,工业上可以用氟化氢气体、氢氧化铝和纯碱在高温条件下发生反应来制取冰晶石,写出该反应的化学方程式: 。 
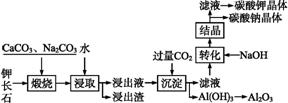
 Al(OH)3+OH-。“浸取”时,应保持溶液呈 (填“酸”或“碱”)性。“浸取”时不断搅拌的目的是 。
Al(OH)3+OH-。“浸取”时,应保持溶液呈 (填“酸”或“碱”)性。“浸取”时不断搅拌的目的是 。