部分弱酸的电离平衡常数如下表所示:
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数(25 ℃) | Ka=1.77×10-4 | Ka=4.9×10-10 | Ka1=4.3×10-7 Ka2=5.6×10-11 |
下列选项正确的是( )
A.2CN-+H2O+CO2===2HCN+CO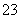
B.中和等体积、等pH的HCOOH和HCN消耗NaOH的量前者小于后者
C.物质的量浓度相等的HCOONa和KCN溶液中,c(Na+)-c(HCOO-)<c(K+)-c(CN-)
D.c(NH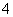 )相等的HCOONH4溶液、NH4CN溶液、NH4HCO3溶液中:c(NH4HCO3)>c(NH4CN)>c(HCOONH4)
)相等的HCOONH4溶液、NH4CN溶液、NH4HCO3溶液中:c(NH4HCO3)>c(NH4CN)>c(HCOONH4)
室温下,将盐酸和氨水等体积混合(忽略体积变化),实验数据如下表:
| 实验编号 | 起始浓度/mol·L-1 | 反应后溶液的pH | |
| c(氨水) | c(HCl) | ||
| ① | 0.1 | 0.1 | 5 |
| ② | 0.2 | x | 7 |
下列叙述错误的是( )
A.实验②反应后的溶液中:c(NH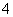 )+c(NH3·H2O)>0.1 mol·L-1
)+c(NH3·H2O)>0.1 mol·L-1
B.实验①反应后的溶液中c(H+)=c(Cl-)+c(OH-)-c(NH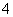 )
)
C.实验①反应后的溶液中:c(Cl-)>c(NH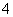 )>c(H+)>c(OH-)
)>c(H+)>c(OH-)
D.实验②反应后的溶液中:c(NH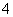 )=c(Cl-)>c(OH-)=c(H+)
)=c(Cl-)>c(OH-)=c(H+)
 )>c(H+)>c(OH-)
)>c(H+)>c(OH-)
 )>c(OH-)>c(H+)
)>c(OH-)>c(H+)

 增大
增大