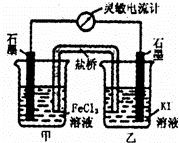
控制适合的条件,将反应2Fe3++2I﹣⇌2Fe2++I2设计成如图所示的原电池.下列判断不正确的是( )
|
| A. | 反应开始时,乙中石墨电极上发生氧化反应 |
|
| B. | 电流计读数为零后,在甲中溶入FeCl2固体,乙中石墨电极为负极 |
|
| C. | 电流计读数为零时,反应达到化学平衡状态 |
|
| D. | 反应开始时,甲中石墨电极上Fe3+被还原 |
锌锰电池以氢氧化钾溶液为电解液,电池总反应式为:Zn(s)+2MnO2(s)+H2O(l)=Zn(OH)2(s)+Mn2O3(s),下列说法错误的是( )
|
| A. | 电路中每通过0.2mol电子,锌的质量理论上减小6.5g |
|
| B. | 电池负极的电极反应式为Zn﹣2e﹣+2 OH﹣=Zn(OH)2 |
|
| C. | 电池工作时,电流由正极通过外电路流向负极 |
|
| D. | 碱性锌锰电池是二次电池 |
在一定条件下,对于A2(g)+3B2(g)⇌2AB3(g)反应来说,以下化学反应速率的表示中,化学反应速率最快的是( )
|
| A. | v(A2)=0.008 mol•L﹣1•s﹣1 | B. | v(A2)=0.3 mol•L﹣1•min﹣1 |
|
| C. | v(AB3)=0.01 mol•L﹣1•s﹣1 | D. | v(B2)=0.012 mol•L﹣1•s﹣1 |
一定条件下用甲烷可以消除氮氧化物(NOx)的污染.已知:
①CH4( g )+4NO2( g )═4NO( g )+CO2( g )+2H2O( g )△H=﹣574kJ•mol﹣1
②CH4( g )+4NO( g )═2N2( g )+CO2( g )+2H2O( g )△H=﹣1160kJ•mol﹣1.
下列正确的选项是( )
|
| A. | CH4(g)+2NO2(g)═N2(g)+CO2(g)+2H2O(l)△H=﹣867kJ•mol﹣1 |
|
| B. | CH4催化还原NOx为N2的过程中,若x=1.6,则转移的电子总数为3.2mol |
|
| C. | 若0.2mol CH4还原NO2至N2,在上述条件下放出的热量为173.4kJ |
|
| D. | 若用标准状况下4.48L CH4还原NO2至N2,整个过程中转移的电子总数为3.2mol |
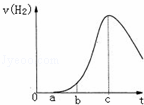
把在空气中久置的铝片5.0g投入盛有 500mL 0.5mol•L﹣1硫酸溶液的烧杯中,该铝片与硫酸反应产生氢气的速率v与反应时间t可用如图的坐标曲线来表示,下列推论错误的是( )
|
| A. | t由0→a段不产生氢气是因为表面的氧化物隔离了铝和硫酸溶液 |
|
| B. | t由b→c段产生氢气的速率增加较快的主要原因之一是温度升高 |
|
| C. | t>c产生氢气的速率降低主要是因为溶液中c(H+)降低 |
|
| D. | t=c时反应处平衡状态 |
某反应A+B=C+D 在低温下能自发进行,在高温下不能自发进行,对该反应过程△H、△S的判断正确的是( )
|
| A. | △H<0△S>0 | B. | △H>0△S>0 | C. | △H<0△S<0 | D. | △H>0△S<0 |
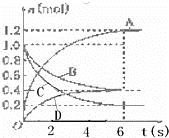
一定温度下,向容积为2L的密闭容器中通入两种气体发生化学反应,反应中各物质的物质的量变化如图所示,对该反应的推断合理的是( )
|
| A. | 该反应的化学方程式为3B+4D⇌6A+2C |
|
| B. | 反应进行到1 s时,v(A)=v(D) |
|
| C. | 反应进行到6 s时,B的平均反应速率为0.05 mol/(L•s) |
|
| D. | 反应进行到6 s时,各物质的反应速率相等 |
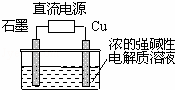
Cu2O是一种半导体材料,基于绿色化学理念设计的制取Cu2O的电解池示意图如图,电解总反应:2Cu+H2O Cu2O+H2↑.下列说法正确的是( )
Cu2O+H2↑.下列说法正确的是( )
|
| A. | 石墨电极上产生氢气 |
|
| B. | 铜电极发生还原反应 |
|
| C. | 铜电极接直流电源的负极 |
|
| D. | 当有0.1mol电子转移时,有0.1molCu2O生成 |
足量镁粉与一定量的盐酸反应,由于反应速率太快,为减慢反应速率,但并不影响氢气产生的总量,可以加入下列物质中的( )
|
| A. | MgO | B. | NaOH | C. | K2CO3 | D. | CH3COONa |



