常温下,用Na2SO3溶液吸收SO2时,溶液pH随n(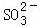 ):n(
):n(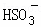 ) 变化的关系如表:
) 变化的关系如表:
| n( | 91:9 | 1:1 | 9:91 |
| pH | 8.2 | 7.2 | 6.2 |
以下离子浓度关系的判断正确的是( )
|
| A. | NaHSO3溶液中c(H+)<c(OH﹣) |
|
| B. | Na2SO3溶液中c(Na+)>c (SO32﹣)>c(HSO3﹣)>c(OH﹣)>c(H+) |
|
| C. | 当吸收液呈中性时,c(Na+)>c(SO32﹣)>c(HSO3﹣)>c(OH﹣)=c(H+) |
|
| D. | 当吸收液呈中性时,c(Na+)=c(HSO3﹣)+2c(SO32﹣) |
下列解释实验事实的方程式不正确的是( )
|
| A. | 葡萄糖的酯化反应若用浓硫酸作催化剂会炭化发黑:C6H12O6(葡萄糖) |
|
| B. | 向AgNO3溶液中加入过量Na2S溶液后,再加NaCl稀溶液,黑色沉淀变成白色:Ag2S+2Cl﹣=2AgCl↓+S2﹣ |
|
| C. | 将NH3通入滴有酚酞的水中,溶液变红:NH3+H2O⇌NH3•H2O⇌NH4++OH﹣ |
|
| D. | 明矾的水溶液pH<7:Al3++3H2O⇌Al(OH)3+3H+ |
异秦皮啶具有镇静安神抗肿瘤功效,秦皮素具有抗痢疾杆菌功效.它们在一定条件下可发生转化,如图所示.有关说法正确的是( )
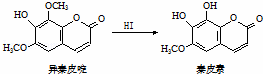
|
| A. | 异秦皮啶与秦皮素互为同系物 |
|
| B. | 异秦皮啶分子式为C11H12O5 |
|
| C. | 秦皮素一定条件下能发生加成反应、消除反应和取代反应 |
|
| D. | 1mol秦皮素最多可与2molBr2、4molNaOH反应 |
下列图象表达正确的是( )
|
| A. |
等质量锌粉与足量盐酸反应 |
|
| B. |
氢气与氧气反应中的能量变化 |
|
| C. |
气态氢化物沸点 |
|
| D. |
催化反应与非催化反应过程中的能量关系 |
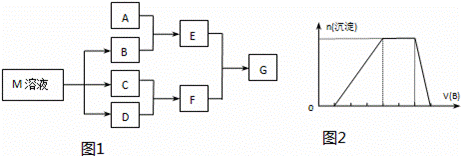
下列实验不是由浊液变清液(溶液)再变浊液的是( )
|
| A. | 大量苯酚和水 |
|
| B. | 大量苯酚和水 |
|
| C. | 硝酸银溶液 |
|
| D. | 碳酸钙和水 |
甲、乙、丙、丁为4种短周期元素,在周期表中,甲与乙、丙、丁在周期表中的位置关系如右图所示(原子序数:乙>丙).丁的原子序数与乙、丙原子序数之和相等,4种元素原子的最外层电子数之和为24.下列判断正确的是( )

|
| A. | 元素甲的简单气态氢化物稳定性比乙的强 |
|
| B. | 元素乙在周期表中的位置为第2周期,VIA族 |
|
| C. | 元素丙和元素丁的最高价氧化物对应的水化物均为强酸 |
|
| D. | 4种元素的简单阴离子半径从大到小顺序为:丁>乙>丙>甲 |
如图是某同学设计的原电池装置,下列叙述中正确的是( )

|
| A. | 电极Ⅰ上发生还原反应,作原电池的负极 |
|
| B. | 电极Ⅱ的电极反应式为:Cu2++2e﹣=Cu |
|
| C. | 该原电池的总反应为:2Fe3++Cu=Cu2++2Fe2+ |
|
| D. | 盐桥中装有含氯化钾的琼脂,其作用是传递电子 |

 )
)  6C+6H2O
6C+6H2O



 苯酚溶液
苯酚溶液 苯酚和水
苯酚和水 苯酚钠溶液
苯酚钠溶液 苯酚
苯酚 氢氧化银和氧化银
氢氧化银和氧化银 银氨溶液
银氨溶液 碳酸氢钙
碳酸氢钙 碳酸钙和水
碳酸钙和水