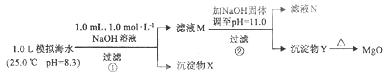
海水中含有丰富的镁资源。某同学设计了从模拟海水中制备MgO的实验方案:
|
| Na+ | Mg2+ | Ca2+ | Cl- | HCO3- |
| 0.439 | 0.050 | 0.011 | 0.560 | 0.001 |
注:溶液中某种离子的浓度小于1.0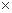 10-5mol
10-5mol L,可认为该离子不存在:
L,可认为该离子不存在:
实验过程中,假设溶液体积不变
Kkp,CaCo3=4.96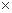 10-9 Kkp,MgCO3=6.82
10-9 Kkp,MgCO3=6.82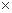 10-6
10-6
Kkp,Ca(OH)2=4.68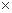 10-9 Kkp,Mg(OH)2=5.61
10-9 Kkp,Mg(OH)2=5.61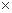 10-12
10-12
下列说法正确的是
A.沉淀物x为CaCO3
B.滤液M中存在Mg2+ ,不存在Ca2+
C.滤液N中存在Mg2+ , Ca2+
D.步骤②中应改为加入4.2g NaOH固体,沉淀物Y为Ca(OH)2和Mg(OH)2的混合物



 2B(g)和2A(g)
2B(g)和2A(g)  2C(g),根据下表中的数据判断下列图像错误的是( )
2C(g),根据下表中的数据判断下列图像错误的是( )
 和OH-
和OH- 2C(g)达平衡后,温度不变,增大压强,平衡正向移动,平衡常数K值增大
2C(g)达平衡后,温度不变,增大压强,平衡正向移动,平衡常数K值增大