纯铁的实际使用范围有限,人们大量使用的是铁的合金.钢铁是铁和钢的总称,其强度高、价格便宜、应用广泛.在以下关于不锈钢和普通钢的认识中,你认为正确的是( )
| A、它们的组成元素是相同的 |
| B、耐腐蚀的性能不同 |
| C、它们都属于钢,因此物理性质是一样的 |
| D、构成普通钢和不锈钢的主要元素是铁,因此它们的化学性质完全相同 |
下列变化中,既属于氧化还原反应又属于吸热反应的是( )
| A、铝和盐酸反应 |
| B、灼热的碳与二氧化碳反应 |
| C、酸碱中和反应 |
| D、氢氧化钡晶体和氯化铵晶体反应 |
若向B、D、F三支试管中分别加入等量的碘液,观察三支试管,发现液体的颜色是蓝色,产生该颜色的原因是( )
| A、淀粉完全水解 |
| B、淀粉部分水解 |
| C、淀粉未能水解 |
| D、淀粉酶与碘反应 |
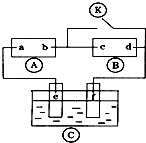 如图
如图 为直流电源,
为直流电源, 为浸透饱和氯化钠溶液和酚酞试液的滤纸,
为浸透饱和氯化钠溶液和酚酞试液的滤纸, 为电镀槽.接通电路后发现
为电镀槽.接通电路后发现 上的c点显红色.为实现铁上镀锌,接通
上的c点显红色.为实现铁上镀锌,接通 后,使c、d两点短路.下列叙述不正确的是( )
后,使c、d两点短路.下列叙述不正确的是( )| A、a为直流电源的正极 |
| B、c极发生的反应为2H++2e-=H2↑ |
| C、f电极为锌板 |
| D、e极发生氧化反应 |
有M、N、P、Z四种金属单质,请根据以下实验:
①P与冷水迅速反应;
②用Pt电极电解同物质的量浓度的M和N的硫酸盐的混合溶液时,在阴极上析出单质N;
③把N和Z用导线相连后,同时浸入Z的硫酸盐溶液中,电极反应是Z2++2e-=Z,N-2e-=N2+.
判断四种金属的活动性顺序是( )
①P与冷水迅速反应;
②用Pt电极电解同物质的量浓度的M和N的硫酸盐的混合溶液时,在阴极上析出单质N;
③把N和Z用导线相连后,同时浸入Z的硫酸盐溶液中,电极反应是Z2++2e-=Z,N-2e-=N2+.
判断四种金属的活动性顺序是( )
| A、M>N>P>Z |
| B、M>N>Z>P |
| C、Z>P>M>N |
| D、P>M>N>Z |
下列说法中不正确的是( )
| A、1molSiO2晶体和1molSi晶体中所含的共价键数之比为2:1 |
| B、在氯化铯晶体中每一个Cs+周围与其等距离且最近的Cl-有8个 |
| C、在氯化钠晶体中每一个Na+距离相等且最近的Cl-所围成的空间几何构型为正八面体 |
| D、水是一种非常稳定的化合物,这是由于水分子间能形成氢键的缘故 |
对于可逆反应M+N?Q达到平衡时,下列说法正确的是( )
| A、M、N、Q三种物质的浓度相同 |
| B、M与N的消耗速率相等 |
| C、M、N、Q的浓度都保持不变 |
| D、反应已经停止 |
下列各组离子在指定溶液中,能大量共存的是( )
①无色溶液中:K+、Na+、MnO4-、SO42-
②pH=13的溶液中:CO32-、Na+、AlO2-、NO3-
③由水电离出的c(H+)=10-12 mol/L的溶液:Ba2+、Na+、NO3-、Cl-
④强酸性溶液中:Fe3+、NO3-、Na+、SO42-
⑤强酸性溶液中:Fe2+、Al3+、NO3-、Cl-.
①无色溶液中:K+、Na+、MnO4-、SO42-
②pH=13的溶液中:CO32-、Na+、AlO2-、NO3-
③由水电离出的c(H+)=10-12 mol/L的溶液:Ba2+、Na+、NO3-、Cl-
④强酸性溶液中:Fe3+、NO3-、Na+、SO42-
⑤强酸性溶液中:Fe2+、Al3+、NO3-、Cl-.
| A、②③④ | B、②④⑤ |
| C、①②⑤ | D、②④ |
对CH3-CH=CH-C≡C-CF3分子结构的下列叙述中,正确的是( )
| A、6个碳原子有可能都在同一直线上 |
| B、在同一直线上的原子至少有5个 |
| C、在同一平面上的原子至少有8个 |
| D、分子中呈四面体结构的碳原子有3个 |
 美国科学家合成了含有N5+的盐类,含有该离子的盐是高能爆炸物质,该离子的结构呈“V”形,如图所示.以下有关该物质的说法中正确的是( )
美国科学家合成了含有N5+的盐类,含有该离子的盐是高能爆炸物质,该离子的结构呈“V”形,如图所示.以下有关该物质的说法中正确的是( )| A、每个N5+中含有35个质子和36个电子 |
| B、该离子中有非极性键和配位键 |
| C、该离子中含有2个π键 |
| D、与PCl4+互为等电子体 |