对同一周期的主族元素的相关性质的叙述,正确的是( )
| A、简单离子的离子半径从左至右逐渐减小 |
| B、最高价氧化物的水化物中这些元素的化合价从左至右逐渐升高 |
| C、单质的熔沸点从左至右逐渐升高 |
| D、能形成简单阴离子的元素的阴离子还原性从左至右逐渐增强 |
有关①100mL 0.01mol?L-1 Na2CO3、②10mL 0.1mol?L-1 Na2CO3两种溶液的叙述正确的是( )
| A、溶液中水电离出的H+个数:②>① |
| B、溶液中阴离子的物质的量浓度之和:①>② |
| C、①溶液中:n(OH-)=n(HCO3-)+2n(H2CO3)+n(H+) |
| D、②溶液中:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) |
 X、Y、Z、W均为中学化学的常见物质,一定条件下它们之间有如图转化关系(其它产物已略去),下列说法不正确的是( )
X、Y、Z、W均为中学化学的常见物质,一定条件下它们之间有如图转化关系(其它产物已略去),下列说法不正确的是( )| A、若W是单质铁,则Z溶液可能是FeCl2溶液 |
| B、若W是氢氧化钠,则X与Z可反应生成Y |
| C、若X是金属铝,则W可能是NaOH溶液 |
| D、若X为甲醇,则X、Z的相对分子质量可能相差14 |
玻璃器皿上沾有一些用水洗不掉的残留物,其洗涤方法不正确的是( )
| A、残留在试管内壁上的碘,用酒精洗涤 |
| B、残留有苯酚的试剂瓶,用酒精洗涤 |
| C、沾附在试管内壁上的油脂,用热碱液洗涤 |
| D、做银镜反应后试管内壁上的银镜,用稀氨水洗涤 |
下列实验操作或对实验事实的叙述正确的是( )
①用稀盐酸洗涤盛放过石灰水的试剂瓶
②配制FeCl3溶液时,向溶液中加入少量Fe粉和稀盐酸
③用pH试纸测得氯水的pH为2
④用稀硝酸清洗做过银镜反应实验的试管
⑤浓硝酸保存在棕色细口瓶中
⑥将镁条和铝片用导线连接再插进稀NaOH溶液,铝条上产生气泡
⑦某溶液加入NaOH并加热能产生使湿润红色石蕊试纸变蓝的气体,则原溶液中含NH4+
⑧清洗试管内壁的MnO2用双氧水.
①用稀盐酸洗涤盛放过石灰水的试剂瓶
②配制FeCl3溶液时,向溶液中加入少量Fe粉和稀盐酸
③用pH试纸测得氯水的pH为2
④用稀硝酸清洗做过银镜反应实验的试管
⑤浓硝酸保存在棕色细口瓶中
⑥将镁条和铝片用导线连接再插进稀NaOH溶液,铝条上产生气泡
⑦某溶液加入NaOH并加热能产生使湿润红色石蕊试纸变蓝的气体,则原溶液中含NH4+
⑧清洗试管内壁的MnO2用双氧水.
| A、①④⑤⑦ | B、②③④⑦ |
| C、①②⑥⑧ | D、①⑤⑥⑧ |
下列有关说法正确的是( )
| A、锂、钛、铁分别位于周期表s、d、ds区 |
| B、CaO的熔点为2614℃,属于原子晶体 |
C、金属铬采取体心立方堆积,则其堆积方式如右图 |
| D、某元素的电负性为1.5,它是金属元素 |
| E、锂、钛、铁分别位于周期表s、d、ds区 |
X+、Y+、Z2-是3种主族元素的离子,X+和Z2-具有相同的电子层结构,Y和Z处于同一周期,关于元素X、Y、Z的下列叙述中不正确的是( )
| A、原子序数:X>Z>Y |
| B、原子半径:Y>Z>X |
| C、离子半径:Z2->X+>Y+ |
| D、一定能形成化合物X2Z |
研究反应物的化学计量数与产物之间的关系时,使用类似数轴的方法可以收到的直观形象的效果.下列表达不正确的是( )
A、CO2通入澄清的石灰水中反应的产物: |
B、Fe在Cl2中的燃烧产物: |
C、AlCl3溶液中滴加NaOH后铝的存在形式: |
D、氨水与SO2反应后溶液中的铵盐: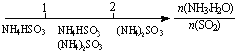 |
在下列条件下不能制得括号中物质的是( )
A、苯在常温下与浓硝酸、浓硫酸混合( ) ) |
| B、溴乙烷在NaOH的水溶液中加热(CH3CH2OH) |
| C、电石中滴加饱和食盐水(C2H2) |
| D、将乙醇和乙酸混合,再加入稀硫酸(CH3COOC2H5) |
金属钫(Fr)天然存在极微量,它的21个已知同位素都具有放射性,它是碱金属元素中最重的元素.根据在周期表中的位置预言其性质,其中不正确的是( )
| A、在已知元素中,它具有最大的原子半径 |
| B、在空气中燃烧时生成化学式为Fr2O的氧化物 |
| C、氧化物的水化物的化学式为FrOH,它应是极强的碱 |
| D、其单质常温下跟水反应比钠剧烈 |