下列叙述中正确的是( )
| A、一切四面体空间构型的分子内键角均为109°28′ |
| B、Cu(OH)2能溶于过量氨水形成络合物[Cu(NH3)4]2+,中心离子为Cu2+,配位体是NH3 |
| C、任何晶体,若含阳离子也一定含阴离子 |
| D、水分子稳定是因为水分子间存在氢键作用 |
下列能源中,属于无污染能源的是( )
| A、煤气 | B、核能 | C、太阳能 | D、石油 |
下列各组物质中,仅用水及物质间相互反应不能一一区别的一组是( )
| A、Na2O2 Al2(SO4)3 MgCl2 K2CO3 |
| B、BaCl2 Na2SO4 (NH4)SO4 KOH |
| C、AgNO3 NaCl KCl CuCl2 |
| D、Fe2(SO4)3 K2CO3 KHSO4 NH4Cl |
能表示阿伏加德罗常数数值的是( )
| A、23g钠在氧气中完全燃烧失电子数为0.5NA |
| B、标准状况下,22.4L苯所含的分子数 |
| C、室温下,8g甲烷含有共价键数为2NA |
| D、1L 1mol?L-1硫酸溶液所含的H+为NA |
下列气态氢化物稳定性最强的是( )
| A、HF |
| B、NH3 |
| C、PH3 |
| D、H2S |
原子序数从11~18的元素,随着核电荷数的递增而逐渐增大的是( )
| A、电子层数 | B、核外电子数 |
| C、原子半径 | D、最外层电子数 |
下列关于离子键的说法中,正确的是( )
| A、阴阳离子间相互吸引即离子键 |
| B、非金属元素所组成的化合物中不可能有离子键 |
| C、一个阳离子只可与一个阴离子之间存在离子键 |
| D、活泼金属与非金属化合时一般形成离子键 |
在硫酸的工业制法中,下列生产操作及说明生产操作的主要原因二者都正确的是( )
| A、从沸腾炉出来的炉气需净化,因为炉气中SO3会与杂质反应 |
| B、硫铁矿燃烧前需要粉碎,因为大块的不能燃烧 |
| C、SO3用98.3%的浓硫酸吸收,目的是防止形成酸雾,以便使SO3吸收完全 |
| D、SO2氧化为SO3时需要使用催化剂,这样可以提高SO2的转化率 |
 如图所示装置中,甲、乙、丙三个烧杯依次分别盛放100g 5.00%的NaOH溶
如图所示装置中,甲、乙、丙三个烧杯依次分别盛放100g 5.00%的NaOH溶液、足量的CuSO4溶液和100g 10.00%的K2SO4溶液,电极均为石墨电极.接通电源,经过一段时间后,测得丙中K2SO4浓度为10.47%,乙中c电极质量增加,计算电极d上生成的气体,在标准状态下体积是( )升.
| A、2.8 | B、5.6 |
| C、8.4 | D、11.2 |
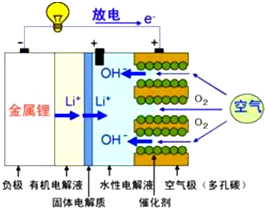 美国IBM公司设计出了一款新型锂空气电池,其原理就是通过吸入空气与设备内的锂离子发生反应,进行能量的提供.因其独特的放电方式,也称呼吸式电池.负极采用金属锂条,负极的电解液采用含有锂盐的有机电解液.中间设有用于隔开正极和负极的锂离子固体电解质.正极的水性电解液使用碱性水溶性凝胶,与由微细化碳和廉价氧化物催化剂形成的正极组合.如图所示.下列说法不正确的是( )
美国IBM公司设计出了一款新型锂空气电池,其原理就是通过吸入空气与设备内的锂离子发生反应,进行能量的提供.因其独特的放电方式,也称呼吸式电池.负极采用金属锂条,负极的电解液采用含有锂盐的有机电解液.中间设有用于隔开正极和负极的锂离子固体电解质.正极的水性电解液使用碱性水溶性凝胶,与由微细化碳和廉价氧化物催化剂形成的正极组合.如图所示.下列说法不正确的是( )| A、负极反应:Li-e-=Li+,金属锂以锂离子(Li+)的形式溶于有机电解液,电子供应给导线.溶解的锂离子(Li+)穿过固体电解质移到正极的水性电解液中 |
| B、正极反应:O2+2H2O+4e-=4OH-,在正极的水性电解液中与锂离子(Li+)结合生成水溶性氢氧化锂(LiOH),并能实现锂元素的循环 |
| C、在负极的有机电解液和空气极的水性电解液之间,用只能通过锂离子的固体电解质隔开,以防止两电解液发生混合,而且能促进电池发生反应 |
| D、锂-空气电池至今都未普及,原因是它存在致命缺陷,即固体反应生成物氧化锂(Li2O)在正极堆积,使电解液与空气的接触被阻断,从而导致放电停止 |