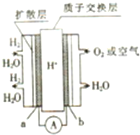
 某质子交换膜燃料电池的工作原理如图所示,其中电极a、b均为多孔活性铂电极,下列手法中不正确的是( )
某质子交换膜燃料电池的工作原理如图所示,其中电极a、b均为多孔活性铂电极,下列手法中不正确的是( )| A、a极为该电池的负极 |
| B、该电池的正极反应式为O2+4e-+2H2O=4OH- |
| C、多孔活性铂电极有利于吸附气体,增大接触面积 |
| D、H+(质子)由负极移向正极 |
近期我国中东部地区发生持续雾霾天气,“PM2.5”数据监测纳入公众视野.PM2.5是指大气中直径小于或等于2.5微米(1微米=10-6米)的可入肺的有害颗粒.下列有关说法不正确的是( )
| A、PM2.5表面积大能吸附大量的有毒、有害物质 |
| B、PM2.5在空气中一定能形成气溶胶 |
| C、与较粗的大气颗粒物相比,PM2.5对人体健康和大气环境质量的影响更大 |
| D、秸秆燃烧、煤炭燃烧、汽车尾气的排放等都与PM2.5的形成有关 |
短周期元素X和Y的原子序数相差6,下列有关判断错误的是( )
| A、X和Y可能位于同一周期或相邻周期 |
| B、X和Y可能位于同一主族或相邻主族 |
| C、X和Y可能形成离子晶体XY |
| D、X和Y可能形成原子晶体XY2 |
 如图是水煤气(成分为CO、H2)空气燃料电池的工作原理示意图,a、b均为惰性电极.下列叙述中正确的是( )
如图是水煤气(成分为CO、H2)空气燃料电池的工作原理示意图,a、b均为惰性电极.下列叙述中正确的是( )| A、A处通入空气,B处通入水煤气 |
| B、a电极的反应式包括:CO+4OH--2e-=CO32-+2H2O |
| C、a电极发生还原反应,b电极发生氧化反应 |
| D、如用这种电池电镀铜,当镀件增重6.4g,则消耗标准状况下的水煤气2.24L |
设NA表示阿伏加德罗常数,下列叙述中正确的是( )
| A、常温常压下,48g O3含有的氧原子数目为3NA |
| B、2.4g金属镁变为离子时失去电子的数目为0.1NA |
| C、含有NA个氦原子的氦气在标准状况下的体积约为11.2L |
| D、物质的量浓度为0.5mol/L MgCl2溶液,含有Cl-离子数目为NA |
下列说法正确的是( )
| A、凡是没有单质参加的化合反应一定是非氧化还原反应 |
| B、有单质参加的反应一定是氧化还原反应 |
| C、凡是有盐参加的反应都是复分解反应 |
| D、置换反应一定是氧化还原反应 |
设NA为阿伏加德罗常数,下列说法正确的是( )
| A、若C2H6分子中含共价键数为7NA,则乙烷的体积为22.4L |
| B、58.5g氯化钠固体中含NaCl分子数为NA |
| C、78g液态笨分子中含碳碳双键数目为3NA |
| D、28g N2和6g H2在高温高压铁触媒催化作用下,生成的NH3分子数一定小于2NA |
下列说法正确的是( )
| A、常温下将pH=2的醋酸和pH=12的NaOH溶液等体积混合,所得溶液显碱性 |
| B、已知同温时氢氟酸的电离常数大于亚硝酸的电离常数,则相同温度相同浓度的NaF溶液和NaNO2溶液的碱性:NaF溶液较强 |
| C、将等体积的盐酸和氨水混合,充分反应后所得溶液呈中性,则两溶液的物质的量浓度关系为:c(HCl)<c(NH3?H2O) |
| D、已知MgCO3的Ksp=6.82×10-6,则所有含有固体MgCO3的溶液中,都有c(Mg2+)=c(CO32-),且c(Mg2+)?c(CO32-)=6.82×10-6 |
下列有关物质的性质和该性质的应用均正确的是( )
| A、常温下浓硫酸与铝不发生反应,可在常温下用铝制容器贮藏贮运浓硫酸 |
| B、二氧化硅不与任何酸反应,可用石英制造耐酸容器 |
| C、二氧化氯具有氧化性,可用于自来水的杀菌消毒 |
| D、铜的金属活泼性比铁的弱,可在海轮外壳上装若干铜块以减缓其腐蚀 |
下列说法合理的是( )
| A、若X+和Y2-的核外电子层结构相同,则原子序数:X>Y |
| B、由水溶液的酸性:HCl>HF,可推断处元素的非金属性越弱,其无氧酸的酸性越强 |
| C、F、Cl、Br、I的氢化物沸点依次升高 |
| D、由两种元素的原子形成的分子中,均只有极性键没有非极性键 |