题目内容
 如图是水煤气(成分为CO、H2)空气燃料电池的工作原理示意图,a、b均为惰性电极.下列叙述中正确的是( )
如图是水煤气(成分为CO、H2)空气燃料电池的工作原理示意图,a、b均为惰性电极.下列叙述中正确的是( )| A、A处通入空气,B处通入水煤气 |
| B、a电极的反应式包括:CO+4OH--2e-=CO32-+2H2O |
| C、a电极发生还原反应,b电极发生氧化反应 |
| D、如用这种电池电镀铜,当镀件增重6.4g,则消耗标准状况下的水煤气2.24L |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:A.燃料电池中,通入燃料的电极失电子、通入氧化剂的电极得电子;
B.a电极上CO和氢气都失电子发生氧化反应;
C.a电极发生氧化反应、b电极发生还原反应;
D.根据转移电子相等进行计算.
B.a电极上CO和氢气都失电子发生氧化反应;
C.a电极发生氧化反应、b电极发生还原反应;
D.根据转移电子相等进行计算.
解答:
解:A.电子的流向可知,电子从a极出来,回到b极,所以a是负极(燃料失电子),b极是正极(O2得电子),故A错误;
B.负极电极反应式:不仅CO失电子,还有H2失电子,CO失电子后变成+4价(以CO2形式存在),而电解质溶液是碱性溶液,所以CO2会与OH-发生反应生成CO32-,故电极反应为:CO+4OH--2e-=CO32-+2H2O,同理可写出H2的反应:H2+2OH--2e-=2H2O,所以漏了H2的反应式,故B错误;
C.a电极是负极,发生氧化反应,b电极是正极,得到电子,发生还原反应,故C错误;
D.如用这种电池电镀铜,当镀件增重6.4gCu,说明n(Cu)=0.1mol.转移n(e-)=0.2mol,1molCO转移2mol e-,1mol H2转移2mol e-,1molCO和H2的混合气体也是转移2mol e-,现增重6.4gCu,转移0.2mol e-,所以消耗CO 0.1mol或0.1mol H2或CO和H2的混合气体0.1mol,故D正确;
故选D.
B.负极电极反应式:不仅CO失电子,还有H2失电子,CO失电子后变成+4价(以CO2形式存在),而电解质溶液是碱性溶液,所以CO2会与OH-发生反应生成CO32-,故电极反应为:CO+4OH--2e-=CO32-+2H2O,同理可写出H2的反应:H2+2OH--2e-=2H2O,所以漏了H2的反应式,故B错误;
C.a电极是负极,发生氧化反应,b电极是正极,得到电子,发生还原反应,故C错误;
D.如用这种电池电镀铜,当镀件增重6.4gCu,说明n(Cu)=0.1mol.转移n(e-)=0.2mol,1molCO转移2mol e-,1mol H2转移2mol e-,1molCO和H2的混合气体也是转移2mol e-,现增重6.4gCu,转移0.2mol e-,所以消耗CO 0.1mol或0.1mol H2或CO和H2的混合气体0.1mol,故D正确;
故选D.
点评:本题考查原电池的工作原理及应用,明确电极反应的判断和电极反应式的书写即可解答,易错选项是D,根据转移电子相等计算,题目难度不大.

练习册系列答案
 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案
相关题目
下列物质中,既含有离子键,又含有极性共价键的是( )
| A、NaCl |
| B、NH4NO3 |
| C、Fe2O3 |
| D、Na2O2 |
下列反应中,不属于氧化还原反应的是( )
| A、CaCO3+2HCl═CaCl2+H2O+CO2↑ | ||||
B、2HClO
| ||||
| C、Cl2+2KI═2KCl+I2 | ||||
D、Cu+2H2SO4(浓)
|
下列有关物质的性质和该性质的应用均正确的是( )
| A、常温下浓硫酸与铝不发生反应,可在常温下用铝制容器贮藏贮运浓硫酸 |
| B、二氧化硅不与任何酸反应,可用石英制造耐酸容器 |
| C、二氧化氯具有氧化性,可用于自来水的杀菌消毒 |
| D、铜的金属活泼性比铁的弱,可在海轮外壳上装若干铜块以减缓其腐蚀 |
恒温恒容的容器内,不可作为可逆反应I2(g)+H2(g)?2HI(g)达到平衡状态的标志的是( )
| A、1 mol H-H键断裂,同时有2 mol H-I键断裂 |
| B、容器内气体的总压强不再变化 |
| C、H2的物质的量浓度不再变化 |
| D、混合气体的颜色不再变化 |
如图所示装置,电流计的指针发生偏转,正极变粗,负极变细,符合这种情况的是( )
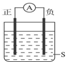

| A、正极Cu,负极Zn,S为稀H2SO4 |
| B、正极Zn,负极Cu,S为CuSO4溶液 |
| C、正极Ag,负极Zn,S为AgNO3溶液 |
| D、正极Fe,负极Cu,S为AgNO3溶液 |
以下比较中,正确的是( )
| A、微粒半径:F->O2->Na+>Li+ |
| B、电负性Cl>C,酸性:HClO4>H2CO3 |
| C、分子中的键角:CH4>H2O>CO2 |
| D、稳定性:LiCl<NaCl<KCl<RbCl |