用NA代表阿伏加德罗常数的值,下列说法正确的是( )
| A、1.0L 1.0mol?L-1 CH3COOH溶液中,CH3COOH分子数为NA |
| B、1mol Na2O2与足量H2O反应转移的电子数NA |
| C、常温常压下,22.4L氧气含有氧原子为2NA |
| D、1.8g重水(D2O)中,含有的质子数为0.1NA |
下列说法不正确的是( )
A、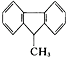 分子中的所有碳原子不可能同时在一个平面内 分子中的所有碳原子不可能同时在一个平面内 |
B、按系统命名法,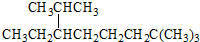 的名称为2,2,7-三甲基-6-乙基辛烷 的名称为2,2,7-三甲基-6-乙基辛烷 |
C、目前市场上大量矿泉水、食用油等产品包装瓶几乎都是用PET(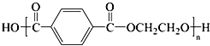 )的合成单体之一是对苯二甲酸 )的合成单体之一是对苯二甲酸 |
| D、有一种信息素的结构简式为CH3(CH2)5CH═CH(CH2)9CHO,为验证该物质中既含有醛基又含有碳碳双键,向该物质的试液中先加过量的溴水溶液,观察到溶液褪色,再向溶液中加入新制的Cu(OH)2悬浊液,加热煮沸,观察到砖红色沉淀 |
下列物质性质的变化规律中与共价键键能大小有关的是( )
①F2、Cl2、Br2、I2的熔点、沸点逐渐升高;②HF、HCl、HBr、HI的热稳定性依次减弱
③金刚石的硬度、熔点、沸点都高于晶体硅;④NaF、NaCl、NaBr、NaI熔点依次降低.
①F2、Cl2、Br2、I2的熔点、沸点逐渐升高;②HF、HCl、HBr、HI的热稳定性依次减弱
③金刚石的硬度、熔点、沸点都高于晶体硅;④NaF、NaCl、NaBr、NaI熔点依次降低.
| A、仅③ | B、①③ | C、②④ | D、②③ |
对于苯乙烯( )的下列叙述:①使溴水反应褪色;②可发生加聚反应;③可溶于苯中;④可溶于水;⑤能发生取代反应;⑥所有的原子可能共平面.其中完全正确的是( )
)的下列叙述:①使溴水反应褪色;②可发生加聚反应;③可溶于苯中;④可溶于水;⑤能发生取代反应;⑥所有的原子可能共平面.其中完全正确的是( )
 )的下列叙述:①使溴水反应褪色;②可发生加聚反应;③可溶于苯中;④可溶于水;⑤能发生取代反应;⑥所有的原子可能共平面.其中完全正确的是( )
)的下列叙述:①使溴水反应褪色;②可发生加聚反应;③可溶于苯中;④可溶于水;⑤能发生取代反应;⑥所有的原子可能共平面.其中完全正确的是( )| A、①②③⑤⑥ | B、①②⑤⑥ |
| C、①②④⑤ | D、①②③④⑤⑥ |
室温时,0.1mol?L-1的HA溶液的pH=3,向该溶液中逐滴加入NaOH,在滴加过程中,有关叙述正确的是( )
| A、原HA溶液中,c(H+)=c(OH-)+c(A-) |
| B、当滴入少量的NaOH,促进了HA的电离,溶液的pH降低 |
| C、当恰好完全中和时,溶液中c(Na+)>c(A-)>c(OH-)>c(H+) |
| D、当NaOH溶液过量时,可能出现:c(A-)>c(Na+)>c(OH-)>c(H+) |
下列离子方程式中正确的是( )
| A、盐酸与碳酸钡反应:CO32-+2H+=CO2↑+H2O |
| B、碳酸钙溶于醋酸:CaCO3+2H+=Ca2++H2O+CO2↑ |
| C、硝酸银溶液中加入铜粉:Ag++Cu=Cu2++Ag |
| D、钠投入水中:2Na+2H2O=2Na++2OH-+H2↑ |
下列分子或离子在指定条件的分散系中
①亚硫酸溶液中:I2、K+、I-、CO32-;
②Ca(NO3)2溶液中:Fe2+、H+、Cl-、SO42-;
③AgI胶体中:S2-、K+、Cl-、NO3-;
④NO2和N2O4的混合气体中:H2O(g)、NH3、Cl2、O2.下列说法正确的是( )
①亚硫酸溶液中:I2、K+、I-、CO32-;
②Ca(NO3)2溶液中:Fe2+、H+、Cl-、SO42-;
③AgI胶体中:S2-、K+、Cl-、NO3-;
④NO2和N2O4的混合气体中:H2O(g)、NH3、Cl2、O2.下列说法正确的是( )
| A、都能大量共存 |
| B、都不能大量共存 |
| C、只有②可以大量共存 |
| D、只有③④可以大量共存 |
某化学科研小组研究在其他条件不变时,改变某一条件对化学平衡的影响,得到如下变化规律(图中P表示压强,T表示温度,n表示物质的量)( )


| A、反应Ⅰ:△H>0,P2>P1 |
| B、反应Ⅱ:△H>0,T1>T2 |
| C、反应Ⅲ:△H>0,T2>T1;或△H<0,T2<T1 |
| D、反应Ⅳ:△H<0,T2>T1 |
有①Na2CO3溶液;②CH3COONa溶液、③NaOH溶液各25mL,物质的量浓度均为0.1mol/L,下列说法正确的是( )
| A、三种溶液pH的大小顺序是③>②>① |
| B、若分别加入25mL 0.1mol/L盐酸后,pH最大的是① |
| C、若将三种溶液稀释相同倍数,pH变化最大的是② |
| D、水电离出的氢离子浓度大小顺序是②>①>③ |
 如图是周期表中短周期的一部分,W、X、Y三种元素原子核外电子数之和等于X的质量数,X原子核内质子数和中子数相等.下列叙述中不正确的是( )
如图是周期表中短周期的一部分,W、X、Y三种元素原子核外电子数之和等于X的质量数,X原子核内质子数和中子数相等.下列叙述中不正确的是( )| A、三种元素的原子半径的大小顺序是W<Y<X |
| B、X元素的氧化物、氢化物的水溶液都呈酸性 |
| C、Y元素的单质是非金属单质中唯一能跟水发生激烈反应的单质 |
| D、W最高价氧化物对应水化物具有强酸性,气态氢化物的水溶液具有弱碱性 |