下列各对化合物中,化学键与晶体类型都相同的一组是( )
| A、H2S、HCl |
| B、NaCl、HF |
| C、SiO2、CO2 |
| D、CCl4、KCl |
关于溶液的下列说法正确的是( )
| A、用湿润的pH试纸测稀碱液的pH,测定值偏大 |
| B、NaCl溶液和CH3COONH4溶液均显中性,两溶液中水的电离程度相同 |
| C、已知:H2B?H++HB-,HB-?H++B2-(电离常数K1=1.3×10-7,K2=7.1×10-15),则NaHB溶液显酸性 |
| D、除去工业废水中的Cu2+可以选用FeS作沉淀剂 |
下列化学药品与其危险化学品图形标志不一致的一组是( )
A、 烧碱--1 |
B、 甲烷--2 |
C、 酒精--3 |
D、 白磷--4 |
镉镍可充电电池工作化学原理如下:Cd+2NiO(OH)+2H2O
Cd(OH)2+2Ni(OH)2,由此可知,该电池放电时的正极是( )
| 充电 |
| 放电 |
| A、Cd |
| B、NiO(OH) |
| C、Cd(OH)2 |
| D、Ni(OH)2 |
下列反应中,HCl既表现出酸性又表现出氧化性的是( )
| A、Zn+2HCl=ZnCl2+H2↑ | ||||
B、2HCl
| ||||
C、MnO2+4HCl(浓)
| ||||
| D、HCl+AgNO3=AgCl↓+HNO3 |
向含有0.078mol FeSO4的溶液中通入201.6mL(标准状况)Cl2,再加入含有0.01mol X2O72-的溶液后,Fe2+恰好完全转化为Fe3+,则反应后X元素的化合价为( )
| A、+3 | B、+4 | C、+5 | D、+6 |
NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A、非标准状况下,1mol任何气体的体积不可能为22.4L |
| B、常温常压下,0.2mol Na2O2与足量H2O反应,转移电子的数目为0.2NA |
| C、标准状况下,NA个水分子所占的体积为22.4L |
| D、常温常压下,0.2mol Na2O2含有0.4mol阴离子 |
常温下,对于①0.1mol/L CH3COOH溶液 ②pH=1HCl溶液 ③pH=13的NaOH溶液 ④0.1mol/L CH3COONa溶液,下列说法正确的是( )
| A、①和②分别稀释100倍后的pH:②>① | ||
| B、水电离出的c(OH-):④>③>①>② | ||
C、①和③混合后溶液呈中性:
| ||
D、①和④混合后溶液呈酸性:
|
T℃时,将气体X与气体Y置于一密闭容器中,反应生成气体Z,反应过程中各物质的 浓度变化如图(Ⅰ)所示.保持其它条件不变,在T1、T2两种温度下,Y的体积分数变化如图(Ⅱ)所示,下列结论正确的是( )
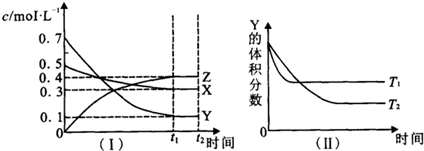

| A、图(Ⅱ)中T1>T2,则正反应是吸热反应 |
| B、t2 min时,保持压强不变,通入稀有气体,平衡向正反应方向移动 |
| C、其它条件不变,升高温度,正、逆反应速率均增大,且X的转化率增大 |
| D、T℃时,若密闭容器中各物质起始浓度为:0.4mol?L-1 X、0.4mol?L-1 Y、0.2mol/L Z保持其他条件不变,达到平衡时z的浓度为0.4 mol?L-1 |