0 134700 134708 134714 134718 134724 134726 134730 134736 134738 134744 134750 134754 134756 134760 134766 134768 134774 134778 134780 134784 134786 134790 134792 134794 134795 134796 134798 134799 134800 134802 134804 134808 134810 134814 134816 134820 134826 134828 134834 134838 134840 134844 134850 134856 134858 134864 134868 134870 134876 134880 134886 134894 203614
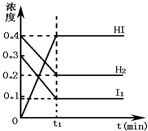 可逆反应H2(g)+I2(g)?2HI(g)在一定的条件下反应混合物中各组分的浓度(mol?L-1)与时间t(min)的变化曲线如图所示,根据图示,回答:
可逆反应H2(g)+I2(g)?2HI(g)在一定的条件下反应混合物中各组分的浓度(mol?L-1)与时间t(min)的变化曲线如图所示,根据图示,回答: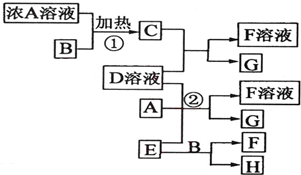
 A、B两种固体物质的溶解度曲线如图所示.请回答:
A、B两种固体物质的溶解度曲线如图所示.请回答:

