NA表示阿伏加德罗常数,下列说法正确的是( )
| A、1mol H2和O2的混合气体中含NA个分子 |
| B、含1mol HCl的盐酸中离子总数为NA个 |
| C、标准状况下11.2L的水中含有0.5个NA水分子 |
| D、在常温常压下,含0.5NA个N原子的氮气所占的体积约为11.2L |
下列说法或表示方法正确的是( )
| A、测定HCl和NaOH的中和热时,每次实验均应测量三个温度,即盐酸的起始温度、NaOH的起始温度和反应结束后稳定的温度 |
| B、31g红磷变成31g白磷要吸收能量,说明白磷比红磷更稳定 |
| C、在101 kPa时,已知氢气的燃烧热为285.8kJ/mol,则氢气燃烧的热化学方程式表示为2H2(g)+O2(g)═2H2O(g)△H=-571.6 kJ/mol |
| D、2A(l)+B(l)=2C(l)△H1 2A (g)+B(g)=2C(l)△H2 则△H1>△H2 |
 在一定温度下,反应:A(s)+3B(g)、xC(g)+2D(g)在一恒压容器中进行,下列说法中正确的是( )
在一定温度下,反应:A(s)+3B(g)、xC(g)+2D(g)在一恒压容器中进行,下列说法中正确的是( )| A、单位时间内生成n mol B,同时生成n mol D,则反应逆向进行 |
| B、当气体体积不变时,说明反应已达到平衡 |
| C、若反应时气体体积增加,则x必大于1且反应一定正向进行 |
| D、若x等于1,不论反应是否平衡,混合气的体积和质量均不会改变 |
有关焰色反应的实验操作注意事项的说明有:①钾的焰色要透过蓝色钴玻璃观察;②先将洗净的铂丝灼烧到与原火焰颜色相同,再蘸取被检物质;③每次实验完,均要用盐酸洗净铂丝.其中正确的是( )
| A、只有① | B、只有③ |
| C、只有①② | D、全部 |
镍(Ni)镉(Cd)可充电的电池,放电时,电极材料是Cd和NiO(OH),电解质是KOH,电极反应分别是:
Cd+2OH--2e-=Cd(OH)2;2NiO(OH)+2H2O+2e-=2Ni(OH)2+2OH-.下列说法不正确的是( )
Cd+2OH--2e-=Cd(OH)2;2NiO(OH)+2H2O+2e-=2Ni(OH)2+2OH-.下列说法不正确的是( )
| A、电池放电时,负极周围溶液的pH不断减小 |
| B、电池放电时总反应是Cd+2NiO(OH)+2H2O=Cd(OH)2+2Ni(OH)2 |
| C、电池充电时,镉(Cd)元素被氧化 |
| D、电池充电时,电池的正极和电源的正极相连接 |
下列装置中能构成原电池的是( )
A、 稀硫酸 稀硫酸 |
B、 稀硫酸 稀硫酸 |
C、 稀硫酸 稀硫酸 |
D、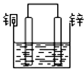 酒精 酒精 |
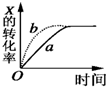
 一定温度下测得在2L的容器中,N、M、P三种气体物质的量的变化如图所示,则有关该反应的说法正确的是( )
一定温度下测得在2L的容器中,N、M、P三种气体物质的量的变化如图所示,则有关该反应的说法正确的是( )| A、该温度下的平衡常数为7.5 |
| B、若升高温度,测得N的转化率减小,则该反应的正反应为吸热反应 |
| C、t3时,正反应速率等于逆反应速率 |
| D、若测得该反应在一段时间内压强不变,说明反应达到平衡 |
下列关于能量转换的认识中不正确的是( )
| A、原电池工作时化学能全部转化为电能 |
| B、工业上电解氧化铝制备铝,电能转化成化学能 |
| C、镁在空气中燃烧时化学能不只转变成热能 |
| D、绿色植物光合作用过程中太阳能转变成化学能 |
含有6.02×1022个分子的某物质的质量为2.8g,则该物质的相对分子质量为( )
| A、14 | B、28 |
| C、2.8 | D、280 |
 随着人类活动加剧,美丽的大自然也受到了一定破坏.“建梦想花园,美一方净土”成为每一个地球人的共同愿望,下列气体中,任意排放会对大气造成严重污染的是( )
随着人类活动加剧,美丽的大自然也受到了一定破坏.“建梦想花园,美一方净土”成为每一个地球人的共同愿望,下列气体中,任意排放会对大气造成严重污染的是( )| A、CO2 |
| B、H2 |
| C、Cl2 |
| D、N2 |