生物学家借助新的显微技术,成功观察到小于20nm的微粒.下列分散系中分散质粒子直径最小的是 (1nm=1x10-9m)( )
| A、雾 |
| B、氢氧化铁胶体 |
| C、石灰乳 |
| D、KNO3溶液 |
下列分离或除杂的方法不正确的是( )
| A、用分液法分离水和酒精 |
| B、用蒸馏法分离苯和溴苯 |
| C、用过滤方法提纯苯甲酸 |
| D、用饱和碳酸氢钠溶液除去二氧化碳中混有的少量氯化氢气体 |
NH3、H2O等是极性分子,CO2、BF3、CCl4等是极性键构成的非极性分子.根据上述事实可推出ABn型分子是非极性分子的经验规律是( )
| A、在ABn分子中A原子的所有价电子都参与成键 |
| B、在ABn分子中A的相对原子质量应小于B的相对原子质量 |
| C、在ABn分子中每个共价键的键长都相等 |
| D、分子中不能含有H原子 |
两种气态烃组成的混合气体0.1mol,完全燃烧得0.2mol CO2和3.6g H2O,则下列关于混合气体组成的说法中不正确的是( )
| A、可能有甲烷 |
| B、可能有乙烯 |
| C、可能有乙烷 |
| D、可能有乙炔 |
已知H-H键的键能为436kJ/mol,Cl-Cl键的键能为243kJ/mol,H-Cl键的键能为431kJ/mol,则H2(g)+Cl2(g)═2HCl(g)的反应热(△H)等于( )
| A、862kJ/mol |
| B、183kJ/mol |
| C、-862kJ/mol |
| D、-183kJ/mol |
下列溶液中,跟100mL 0.5mol/L CaCl2溶液所含的Cl-物质的量浓度相同的是( )
| A、100mL 1mol/L MgCl2溶液 |
| B、200mL 0.25mol/L AlCl3溶液 |
| C、100ml 1mol/L NaCl溶液 |
| D、200ml 0.5mol/L HCl溶液 |
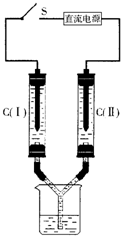 如图所示装置,两玻璃管中盛满滴有酚酞溶液的NaCl饱和溶液,C(Ⅰ)、C(Ⅱ)为多孔石墨电极.接通S后,C(Ⅱ)附近溶液变红,两玻璃管中有气体生成.下列说法正确的是( )
如图所示装置,两玻璃管中盛满滴有酚酞溶液的NaCl饱和溶液,C(Ⅰ)、C(Ⅱ)为多孔石墨电极.接通S后,C(Ⅱ)附近溶液变红,两玻璃管中有气体生成.下列说法正确的是( )| A、C(Ⅰ)电极产生可燃性气体 | ||||
| B、C(Ⅱ)的电极附近溶液呈碱性 | ||||
| C、C(Ⅱ) 电极产生的气体可使湿润的碘化钾淀粉试纸变蓝色 | ||||
D、电解过程中发生的化学方程式为:2NaCl
|
上世纪80年代后期,人们发现NO在人体内起着多方面重要的生理作用.下列关于NO的说法错误的是( )
| A、NO是汽车尾气的有害成分之一 |
| B、NO是具有刺激性气味的红棕色气体 |
| C、NO极少量时在人体的血管系统内会促进血管扩张,防止血管栓塞 |
| D、NO能够与人体血红蛋白结合,吸入较多会造成人体缺氧中毒 |
下列说法正确的是( )
| A、金属与盐溶液间的反应一定是置换反应 | ||||
| B、能与酸反应的氧化物一定是碱性氧化物 | ||||
C、
| ||||
| D、常见金属铁和铝在工业上是由热还原法制得的 |