设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A、常温常压下,17g甲基(-14CH3)所含的电子数为10NA |
| B、pH=1的稀硫酸中含有的H+数为0.1NA |
| C、7.8g过氧化钠与足量二氧化碳反应转移的电子数为0.1NA |
| D、3mol NO2和足量H2O反应,转移NA个电子 |
在一个不导热的密闭反应器中,只发生两个反应:a(g)+b(g)?2c(g)△H<0,x(g)+3y(g)?2z(g)△H>0进行相关操作且达到平衡后(忽略体积改变所做的功),下列叙述正确的是( )
| A、恒容时,通入x气体,y的物质的量浓度增大 |
| B、恒容时,通入x气体,反应器中温度升高 |
| C、恒容时,通入惰性气体,各反应速率不变 |
| D、恒压时,通入惰性气体,c的物质的量不变 |
下列叙述正确的是( )
| A、N2+3H2?2NH3 △H<0,升高温度,逆反应速率加快,正反应速率减慢 |
| B、在稀溶液中,H+(aq)+OH-(aq)═H2O(l);△H=-57.3kJ?mol-1,若将含0.5molH2SO4的浓硫酸与含1mol NaOH的溶液混合,放出的热量为57.3 kJ |
| C、由C(石墨)═C(金刚石);△H=+1.90kJ?mol-1可知,金刚石比石墨稳定 |
| D、纯锌与稀硫酸反应时,加入少量CuSO4溶液,可使反应速率加快 |
下列离子方程式正确的是( )
| A、工业制取漂白粉:2Cl2+4OH-=2Cl-+2ClO-+2H2O | ||
B、向NaOH溶液中滴加同浓度的少量Ca(HCO3)2溶液:Ca2++HCO
| ||
| C、硫酸亚铁加过氧化氢溶液:Fe2++H2O2+2H+═Fe3++4H2O | ||
| D、铝粉与NaOH的D2O溶液反应:2Al+2OH-+2D2O═2AlO2-+3D2↑ |
在下列反应中:aFeS+bH2SO4(浓)→cFe2(SO4)3+dSO2+eS↓+6H2O,a、b数值是( )
| A、a=2,b=6 |
| B、a=4,b=18 |
| C、a=6,b=16 |
| D、a=8,b=18 |
下列说法正确的是( )
| A、SiO2制成的玻璃纤维,由于导电能力强而被用于制造通讯光缆 |
| B、由于Fe可被浓H2SO4氧化,因此常温下不能用钢瓶贮浓H2SO4 |
| C、镁铝合金的熔点比镁和铝都高 |
| D、不能用氨水鉴别Al3+﹑Mg2+﹑Ag+ |
下列叙述不正确的是( )
| A、由分子构成的物质其熔点一般较低 |
| B、分子晶体在熔化时,共价键没有被破坏 |
| C、分子晶体中一定存在共价键 |
| D、分子晶体中分子间作用力越大,其化学性质越稳定 |
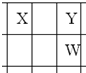 X、Y、Z、W、Q是原子序数依次增大的五种短周期主族元素.其中只有Z是金属,W的单质是黄色固体,X、Y、W在周期表中的相对位置关系如图所示.下列说法正确的是( )
X、Y、Z、W、Q是原子序数依次增大的五种短周期主族元素.其中只有Z是金属,W的单质是黄色固体,X、Y、W在周期表中的相对位置关系如图所示.下列说法正确的是( )| A、五种元素中,原子半径最大的是W |
| B、Y的简单阴离子比W的简单阴离子还原性强 |
| C、Y与Z形成的化合物都可以和盐酸反应 |
| D、X与Q形成的化合物是离子化合物 |
pH=11的X、Y两种碱溶液各10mL,分别稀释至1000mL,此时pH(Y)>pH(X),下列说法中正确的是( )
| A、若X、Y两种碱溶液都是一元碱,则X、Y两种溶液的物质的量浓度一定相等 |
| B、稀释后X溶液中水电离的c(H+)比Y溶液中水电离的c(H+)小 |
| C、若稀释后两溶液的9<pH<11,则X、Y都是弱碱 |
| D、完全中和X、Y两溶液时,消耗同浓度盐酸的体积V(X)>V(Y) |