下列有关金属铝及其化合物的叙述正确的是( )
| A、铝片在空气能与氧气剧烈燃烧并放出大量的热 |
| B、工业上用电解氯化铝生产铝 |
| C、氢氧化铝在溶液中只能电离出铝离子 |
| D、硫酸铝钾溶液中滴入足量的氢氧化钡溶液,则得到的沉淀只有硫酸钡 |
分类是学习和研究化学的一种常用的科学方法.下列分类合理的是( )
①根据元素原子最外层电子数的多少将元素分为金属元素和非金属元素
②根据反应中是否有电子的转移将化学反应分为氧化还原反应和非氧化还原反应
③根据电解质在熔融状态下能否完全电离将电解质分为强电解质和弱电解质.
①根据元素原子最外层电子数的多少将元素分为金属元素和非金属元素
②根据反应中是否有电子的转移将化学反应分为氧化还原反应和非氧化还原反应
③根据电解质在熔融状态下能否完全电离将电解质分为强电解质和弱电解质.
| A、①② | B、①③ | C、② | D、①②③ |
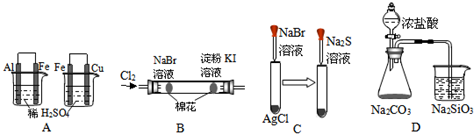
下列叙述中正确的是( )
| A、某溶液加入BaCl2溶液,产生不溶于稀硝酸的白色沉淀,该溶液一定含有Ag+ |
| B、液溴易挥发,在存放液溴的试剂瓶中应加水封 |
| C、某溶液加入CCl4,CCl4层显紫色,证明原溶液中存在I- |
| D、能使润湿的淀粉KI试纸变成蓝色的物质一定是Cl2 |
可逆反应:2NO2?2NO+O2在一体积固定的密闭容器中进行,其达到平衡状态的标志是( )
①单位时间内生成nmolO2的同时也生成了2nmol NO2
②单位时间内生成nmolO2的同时也生成了2nmol NO
③用NO2、NO、O2 表示的反应速率之比为2:2:1
④混合气体的颜色不再改变
⑤混合气体的密度不再改变
⑥混合气体的压强不再改变
⑦混合气体的平均相对分子质量不再改变.
①单位时间内生成nmolO2的同时也生成了2nmol NO2
②单位时间内生成nmolO2的同时也生成了2nmol NO
③用NO2、NO、O2 表示的反应速率之比为2:2:1
④混合气体的颜色不再改变
⑤混合气体的密度不再改变
⑥混合气体的压强不再改变
⑦混合气体的平均相对分子质量不再改变.
| A、①④⑥⑦ | B、②③⑤⑦ |
| C、①③④⑤ | D、全部 |
二氯化二硫(S2C12)可用作橡胶工业的硫化剂,常温下它是橙黄色有恶臭的液体,它的分子结构与H202相似,熔点为l93K,沸点为41lK,遇水很容易水解,产生的气体能使品红褪色,S2C12可由干燥的氯气通入熔融的硫中制得.下列有关说法正确的是( )
| A、S2C12晶体中不存在离子键 |
| B、S2C12分子中各原子均达到8电子稳定结构 |
| C、S2C12在熔融状态下能导电 |
| D、S2C12与水反应后生成的气体难溶于水 |
下列操作达到预期目的是( )
①甲烷中含有乙烯,可以通入溴水达到除去乙烯
②用酸性高锰酸钾溶液除去乙炔中含有的H2S
③用乙醇和3%的硫酸共热到170℃制取乙烯
④甲烷和氯气混合光照可以制取纯净一氯甲烷
⑤将敞口久置的电石与蒸馏水混合制乙炔.
①甲烷中含有乙烯,可以通入溴水达到除去乙烯
②用酸性高锰酸钾溶液除去乙炔中含有的H2S
③用乙醇和3%的硫酸共热到170℃制取乙烯
④甲烷和氯气混合光照可以制取纯净一氯甲烷
⑤将敞口久置的电石与蒸馏水混合制乙炔.
| A、只有① | B、只有③④⑤ |
| C、只有①②③⑤ | D、都不行 |
用NA表示阿伏加德罗常数的值,下列叙述中正确的是( )
| A、100mL 0.1mol?L-1的稀硫酸中含有SO42-的个数为0.1NA |
| B、每有1mol Fe参加氧化还原反应失去电子数目均为2NA |
| C、标准状况下,22.4L水所含水分子数为NA |
| D、标准状况下,足量锌与稀硫酸反应每生成1mol氢气转移电子数为2NA |
氰气的化学式为(CN)2,它的性质和卤素相似,称为拟卤素,对其性质和有关化合物性质的叙述不正确的是( )
| A、HCl和HCN都易形成白雾 |
| B、(CN)2和NaOH溶液反应生成NaCN、NaCNO和H2O |
| C、NaCN和AgCN都易溶于水 |
| D、MnO2可与浓HCN溶液反应生成(CN)2 |
如图是某硫酸试剂瓶标签上的部分内容,据此判断下列说法不正确的是( )


| A、该硫酸的物质的量浓度为l8.4mol/L |
| B、该硫酸与等体积的水混合所得溶液的质量分数大于49% |
| C、配制200.0mL4.6mol/L的稀硫酸需取该硫酸50.0mL |
| D、6.4gCu与足量的该硫酸充分反应产生的气体一定为2.24L |