题目内容
氰气的化学式为(CN)2,它的性质和卤素相似,称为拟卤素,对其性质和有关化合物性质的叙述不正确的是( )
| A、HCl和HCN都易形成白雾 |
| B、(CN)2和NaOH溶液反应生成NaCN、NaCNO和H2O |
| C、NaCN和AgCN都易溶于水 |
| D、MnO2可与浓HCN溶液反应生成(CN)2 |
考点:卤素原子结构及其性质的比较
专题:信息给予题
分析:拟卤素性质和卤素性质相似,根据卤素单质、卤化物、氯气的制取方法分析氰气的性质、制取方法.
解答:
解:A.HCl遇水蒸气易形成盐酸小液滴,所以HCN遇水蒸气也能形成该酸的小液滴,则能形成白雾,故A正确;
B.氯气和NaOH溶液反应生成NaCl、NaClO、H2O,根据性质的相似性知,(CN)2和NaOH溶液反应生成NaCN、NaCNO和H2O,故B正确;
C.AgCl不易溶于水,根据物质的相似性知,AgCN不溶于水,故C错误;
D.二氧化锰和浓盐酸在加热条件下反应生成氯气,根据物质的相似性知,MnO2可与浓HCN溶液反应生成(CN)2,故D正确;
故选C.
B.氯气和NaOH溶液反应生成NaCl、NaClO、H2O,根据性质的相似性知,(CN)2和NaOH溶液反应生成NaCN、NaCNO和H2O,故B正确;
C.AgCl不易溶于水,根据物质的相似性知,AgCN不溶于水,故C错误;
D.二氧化锰和浓盐酸在加热条件下反应生成氯气,根据物质的相似性知,MnO2可与浓HCN溶液反应生成(CN)2,故D正确;
故选C.
点评:本题考查物质的性质,正确理解题给信息是解本题关键,利用知识迁移的方法以氯气的性质及制取为例分析氰气的性质,注意卤化银中AgF能溶于水,为易错点.

练习册系列答案
 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案
相关题目
下列离子方程式中书写正确的是( )
| A、FeCl2溶液中通入Cl2:Fe2++Cl2═Fe3++2Cl- |
| B、Al2O3与NaOH溶液反应:Al2O3+2OH-═2[Al(OH)4]- |
| C、FeCl3溶液与铜:Fe3++Cu═Fe2++Cu2+ |
| D、用醋酸除水垢:2CH3COOH+CaCO3═2CH3COO-+Ca2++H2O+CO2↑ |
根据相关的化学原理,下列判断正确的是( )
| A、由于水中存在氢键,所以稳定性:H2O>H2S |
| B、由于非金属性F>Cl>Br>I,所以酸性:HF>HCl>HBr>HI |
| C、分散质粒子直径:Fe(OH)3悬浊液>Fe(OH)3胶体>FeCl3溶液 |
| D、若R2-和M+的电子层结构相同,则原子半径 R>M |
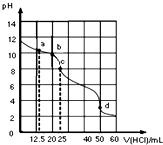 在常温下,0.1000mol?L-1Na2CO3溶液25mL 用0.1000mol?L-1盐酸滴定,其滴定曲线如图.对滴定过程中所得溶液中相关离子浓度间的关系,下列有关说法正确的是( )
在常温下,0.1000mol?L-1Na2CO3溶液25mL 用0.1000mol?L-1盐酸滴定,其滴定曲线如图.对滴定过程中所得溶液中相关离子浓度间的关系,下列有关说法正确的是( )| A、a点:c(CO32-)=c(HCO3-)>c(OH-) |
| B、b点:5c(Cl-)=4c(HCO3-a点:c(CO32-)=c(HCO3-)>c(OH-))+4c(CO32-) |
| C、c点:c(OH-)+c(CO32-)=c(H+)+c(H2CO3) |
| D、d点:c(Na+)<c(Cl-)+ |
下列图示与对应的叙述相符的是( )
A、 说明烯烃与H2的加成反应是放热反应,虚线表示在有催化剂的条件下进行 |
B、 用0.1000mol/LNaOH溶液分别滴定浓度相同的三种一元酸,由图曲线可确定①的酸性最强 |
C、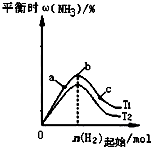 图表示合成氨反应在其他条件不变的情况下,改变n(H2)起始对平衡的影响.由此可知,N2的转化率最高的是b点;且T1>T2,K2>K1(T1和T2表示温度,K1、K2表示对应温度下的平衡常数) |
D、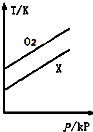 在体积相同的两个密闭容器中,分别充入等质量的O2和X气体,由图可确定X可能是CH4 |
对于反应8LiCoO2+Na2S2O3+□ =4Li2SO4+8CoSO4+Na2SO4+□ ,下列说法正确的是( )
| A、Na2S2O3在反应中被还原为Na2SO4 |
| B、0.1mol Na2S2O3在反应中转移0.4mol电子 |
| C、反应中的未知物的系数均为11 |
| D、还原性LiCoO2大于CoSO4 |
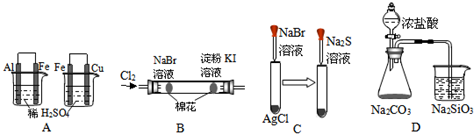
下列实验装置图正确的是( )
A、 实验室制乙烯 |
B、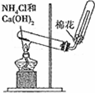 实验室制氨气 |
C、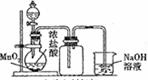 实验室制氯气 |
D、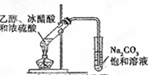 实验室制乙酸乙酯 |
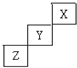 短周期元素X、Y、Z在周期表中的位置关系如图所示,回答下列问题:
短周期元素X、Y、Z在周期表中的位置关系如图所示,回答下列问题: