比较形状和质量相同的两块硫黄分别在空气和氧气中燃烧的实验,下列说法中不正确的是( )
| A、在氧气中比在空气中燃烧得更旺 |
| B、在氧气中火焰为明亮的蓝紫色 |
| C、在氧气中反应比在空气中反应速率快 |
| D、在氧气中燃烧比在空气中燃烧放出的热量多 |
一定条件下,在体积为10L的密闭容器中,1molX和1molY发生反应:2x(g)+Y(g)?Z(g),经60s达到平衡,生成0.3mol Z.下列说法正确的是( )
| A、反应进行30 s时,正反应速率等于逆反应速率 |
| B、反应进行80 s时,逆反应速率大于正反应速率 |
| C、反应进行60 s时,X的物质的量浓度为0.04 mol/L |
| D、反应进行60 s时,Y的转化率为70% |
阿伏加德罗常数约为6.02×1023mol-1,用NA表示,下列说法中一定正确的是( )
| A、100mL 2.0mol/L的盐酸溶液中氢离子数为2NA |
| B、0.1mol CH4所含的电子数为1NA |
| C、Na2O2与H2O反应生成1.12LO2(标准状况),反应中转移的电子数为2×6.02×1022 |
| D、标准状况下,22.4L Cl2和HCl的混合气体中含分子总数为2×6.02×1023 |
下列基本的实验操作不正确的是( )
A、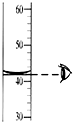 液体体积读数 |
B、 熄灭酒精灯 |
C、 检查气密性 |
D、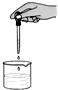 滴加液体 |
恒温下,对于定容密闭容器中进行的反应:H2(g)+I2(g)?2HI(g),下列说法能充分说明该反应已达到化学平衡状态的是( )
| A、正、逆反应速率都等于零 |
| B、体系颜色不变 |
| C、H2、I2、HI在容器中共存 |
| D、混合气体密度不变 |
下列说法正确的是( )
| A、甲苯分子中所有原子都处于同一平面内 |
| B、1个苯分子中含有3个碳碳双键 |
| C、乙烯和苯都能使溴水褪色,褪色的原理相同 |
| D、100 g质量分数为46%的乙醇溶液中,共有14 mol共价键 |
下列各表述与示意图图中一致的是( )


| A、图①表示向含Mg2+、Al3+、NH4+的盐溶液中滴加NaOH溶液时,沉淀的量与NaOH的体积的关系图.则三种离子的物质的量之比为:n(Mg2+):n(Al3+):n( NH4+)=2:3:2 |
| B、图①中使用的NaOH的浓度为10 mol/L |
| C、图②表示25℃时,用0.1 mol?L-1盐酸滴定20 mL 0.1 mol?L-1 NaOH溶液,溶液的pH随加入酸体积的变化 |
| D、图③中曲线表示3N2(g)+N2(g)?2NH3(g)反应过程的能量变化,若使用催化剂,B点会升高 |
化学与人类生活、社会可持续发展密切相关,下列措施有利于节能减排、保护环境的是:
①加快化石燃料的开采与使用;
②研发易降解的生物农药;
③应用高效洁净的能源转换技术;
④田间焚烧秸秆;
⑤推广使用节能环保材料;
⑥2M+N=2P+2Q,2P+M=Q(M、N为原料,Q为期望产品)
其中符合“化学反应的绿色化”的要求的是( )
①加快化石燃料的开采与使用;
②研发易降解的生物农药;
③应用高效洁净的能源转换技术;
④田间焚烧秸秆;
⑤推广使用节能环保材料;
⑥2M+N=2P+2Q,2P+M=Q(M、N为原料,Q为期望产品)
其中符合“化学反应的绿色化”的要求的是( )
| A、①③④⑤ | B、②③⑤⑥ |
| C、①②③④ | D、②④⑤⑥ |
A+、B-、C、D四种微粒中均含有氢原子,且电子总数均为18个.已知溶液中的A+和B-在一定条件下相互反应可转化为C和D.则C、D分别为( )
| A、NH3 和H2O |
| B、PH4+和HS- |
| C、NH4+和OH- |
| D、PH3+H2S |