如图图示与对应的叙述相符的是( )


| A、图甲表示在恒容密闭容器中,恒温条件下发生的可逆反应2NO2(g)?N2O4(g),各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态 |
| B、图乙曲线表示反应2A(g)+B(g)?2C(g)△H>0,正、逆反应的平衡常数K随温度的变化 |
| C、图丙表示对反应2X(g)+Y(g)?Z(s)+3W(g)△H<0在t1时刻增大压强 |
| D、图丁表示反应aA(g)+bB(g)?cC(g)+dD(g):a+b>c+d;T1<T2;△H<0 |
实验室用锌粒与2mol?L-1硫酸溶液制取氢气,下列措施不能增大化学反应速率的是( )
| A、向该硫酸溶液中加入少量浓硫酸 |
| B、向该硫酸溶液中加入少量水 |
| C、改用热的2 mol?L-1硫酸溶液 |
| D、用锌粉代替锌粒 |
在一定温度下,可逆反应X(g)+3Y(g)?2Z(g)已达到平衡的标志是( )
| A、单位时间内消耗n mol X同时生成2n mol Z |
| B、X(g)的浓度保持不变 |
| C、X、Y、Z的平衡浓度相等 |
| D、V(X)、V(Y)、V(Z)的之比为1:3:2 |
下列说法正确的是( )
| A、宁波从2012年3月25日起公布了空气中的PM2.5,PM2.5是指空气中细颗粒物直径≤2.5u m(1um=10-6m)的颗粒物,它在空气中能形成气溶胶 |
| B、“可燃冰”的燃烧、从海水中得到溴单质、石油分馏全都是化学变化的过程 |
| C、氯化钠、干冰、纯碱属于晶体,具有规则的几何外形和固定的熔点,石蜡、玻璃属于非晶态物质,没有固定的熔点,也不具备规则的几何外形 |
D、原子结构模型的演变历史可表示为: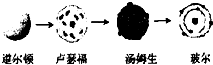 |
设nA代表阿伏加德罗常数(NA)的数值,下列说法正确的是( )
| A、22.4 L Cl2中含有nA个C12分子 |
| B、1 L 0.1 mol?L-1 Na2SO4溶液中有0.2 nA个Na+ |
| C、1 mol H2与1 mol C12反应生成nA个HCl分子 |
| D、1 mol Ca变成Ca2+时失去的电子数为2nA |
已知所含元素化合价发生变化的反应是氧化还原反应,其中被还原的元素化合价降低,被氧化的元素化合价升高.海洋中有丰富的资源,如图所示利用海水可获得许多化工产品.下列说法正确的是( )


| A、第①步中除去粗盐中的SO42-、Ca2+、Mg2+等杂质,加入的试剂顺序为:Na2CO3溶液、NaOH溶液、BaCl2溶液,过滤后加盐酸 |
| B、第②步中加入的试剂为CaCl2溶液 |
| C、第③步中发生分解反应 |
| D、在第④步中溴元素被还原 |
对下列化学反应热现象,不正确的说法是( )
| A、放热的反应,不必加热就能发生反应 |
| B、化学反应一定有能量变化 |
| C、化学反应中,吸热反应不一定需要加热也能发生 |
| D、热化学反应方程式中,反应热与计量数大小有关 |
下列物质中含有原子数由多到少排列正确的是( )
①0.1molH2SO4②4.8g氦气 ③5.6L标况下NH3(气)④4℃时的5.4mLH2O.
①0.1molH2SO4②4.8g氦气 ③5.6L标况下NH3(气)④4℃时的5.4mLH2O.
| A、①②③④ | B、④③②① |
| C、②③④① | D、②④③① |
向11.2g Fe2O3、Cu的混合物中加入0.25mol?L-1的硫酸溶液600mL时,固体恰好完全溶解,溶液中不含Fe3+,若用过量的CO在高温下还原相同质量的原混合物,固体减少的质量为( )
| A、2.4g | B、1.6g |
| C、4.8g | D、6.4g |
下列反应中,一种物质既被氧化又被还原的是( )
| A、2Fe+6H+═2Fe3++3H2↑ | ||||
B、CaCO3
| ||||
| C、Na2CO3+2HCl═2NaCl+CO2↑+H2O | ||||
| D、3NO2+H2O═2HNO3+NO |