题目内容
在一定温度下,可逆反应X(g)+3Y(g)?2Z(g)已达到平衡的标志是( )
| A、单位时间内消耗n mol X同时生成2n mol Z |
| B、X(g)的浓度保持不变 |
| C、X、Y、Z的平衡浓度相等 |
| D、V(X)、V(Y)、V(Z)的之比为1:3:2 |
考点:化学平衡状态的判断
专题:化学平衡专题
分析:化学反应达到化学平衡状态时,正逆反应速率相等,且不等于0,各物质的浓度不再发生变化,由此衍生的一些物理量不发生变化,以此进行判断,得出正确结论.
解答:
解:X(g)+3Y(g)?2Z(g),
A.单位时间内消耗n mol X是正反应,同时生成2n mol Z也正反应,故不能说明达到平衡状态,故A错误;
B.X(g)的浓度保持不变,说明达到平衡状态,故B正确;
C.平衡时各物质的浓度关系取决于物质的起始物质的量和转化率,故X、Y、Z的平衡浓度相等不能作为判断是否达到平衡状态的依据,故C错误;
D.平衡时各物质的体积之比取决于物质的起始物质的量和转化率,故V(X)、V(Y)、V(Z)的之比为1:3:2不能作为判断是否达到平衡状态的依据,故D错误;
故选B.
A.单位时间内消耗n mol X是正反应,同时生成2n mol Z也正反应,故不能说明达到平衡状态,故A错误;
B.X(g)的浓度保持不变,说明达到平衡状态,故B正确;
C.平衡时各物质的浓度关系取决于物质的起始物质的量和转化率,故X、Y、Z的平衡浓度相等不能作为判断是否达到平衡状态的依据,故C错误;
D.平衡时各物质的体积之比取决于物质的起始物质的量和转化率,故V(X)、V(Y)、V(Z)的之比为1:3:2不能作为判断是否达到平衡状态的依据,故D错误;
故选B.
点评:本题考查化学平衡状态的判断,题目难度不大.要注意把握平衡状态的特征.

练习册系列答案
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案
相关题目
烧柴禾时,通常把木柴架空一些才能燃烧更旺,这是因为( )
| A、可以降低着火点 |
| B、散热的速率快 |
| C、木柴是可燃物 |
| D、使柴禾和空气充分接触 |
反应NH4HS(s)?NH3(g)+H2S(g)在一定温度下达到平衡.下列各种情况下,不能使平衡发生移动的是( )
| A、温度、容积不变时,通入SO2气体 |
| B、移走一部分NH4HS固体 |
| C、容积不变,充入氨气 |
| D、充入氮气,保持压强不变 |
已知X、Y、Z为三种原子序数相连的元素,它们最高价氧化物对应水化物的酸性相对强弱是:HXO4>H2YO4>H3ZO4.则下列说法错误的是( )
| A、气态氢化物的稳定性:X>Y>Z |
| B、非金属性:Y<X<Z |
| C、原子半径:X>Y>Z |
| D、原子序数:Z<Y<X |
下列物质中含有原子数由多到少排列正确的是( )
①0.1molH2SO4②4.8g氦气 ③5.6L标况下NH3(气)④4℃时的5.4mLH2O.
①0.1molH2SO4②4.8g氦气 ③5.6L标况下NH3(气)④4℃时的5.4mLH2O.
| A、①②③④ | B、④③②① |
| C、②③④① | D、②④③① |
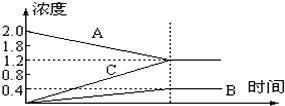 如图曲线是800℃时,A、B、C三种气体物质的浓度随时间变化情况,能以此曲线表示的反应是( )
如图曲线是800℃时,A、B、C三种气体物质的浓度随时间变化情况,能以此曲线表示的反应是( )| A、2A?B+3C |
| B、B+3C?2A |
| C、A+C?B |
| D、A?B+C |
用下列装置进行实验,设计正确且能达到实验目的是( )
A、 制取少量H2 |
B、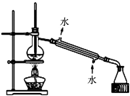 分离Na2CO3溶液和CH3COOC2H5的混合物 |
C、 验证Na和水反应为放热反应 |
D、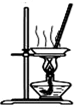 蒸干NH4Cl饱和溶液制备NH4Cl晶体 |
下列相应离子方程式书写错误的是( )
| A、向100 mL浓度为2 mol?L-1 的FeI2溶液中通入5.6 L(标准状况下)的Cl2:4Fe2++8I-+5Cl2=4Fe3++4I2+10Cl- | ||||
| B、Na2S2O3溶液中加入稀硫酸:S2O32-+2H+=SO2↑+S↓+H2O | ||||
| C、将SO2通入酸性KMnO4溶液中:5SO2+2MnO4-+2H2O=5SO42-+2Mn2++4H+ | ||||
D、用惰性电极电解硝酸银溶液:4Ag++2H2O
|
已知:P4(s、白磷)+5O2(g)═P4O10(s)△H=-2983.2kJ/mol;4P(s、红磷)+5O2(g)═P4O10(s)△H=-2954kJ/mol;那么,1mol白磷转变成相应物质的量红磷时,应是( )
| A、吸收29.2kJ热量 |
| B、放出29.2kJ热量 |
| C、放出7.3kJ热量D.吸收7.3kJ热量 |
| D、101 kPa时,1mol碳燃烧所放出的热量为碳的燃烧热 |