将氯酸钾加热分解,在0.5min内放出5mL氧气,加入二氧化锰后,在同样温度下,0.2min内放出50mL氧气.则加入二氧化锰后的反应速率是未加二氧化锰时反应速率的( )
| A、10倍 | B、25倍 |
| C、50倍 | D、250倍 |
若NA代表阿伏加德罗常数的值,则下列叙述中,正确的是( )
| A、一定条件下,足量铜与200 g 98%的浓硫酸充分反应,转移电子数目为2NA | ||
| B、16 g氧气和臭氧的混合气体中含有的氧原子数为NA | ||
C、1 L 0.5 mol?L-1 Na2CO3溶液中含有的CO
| ||
| D、78 g Na2O2中所含阴离子的数目是NA |
硫代硫酸钠(Na2S2O3)与稀H2SO4溶液时发生如下反应:Na2S2O3+H2SO4=Na2SO4+SO2↑+S↓+H2O.下列反应速率最大的是( )
| A、0.1 mol/L Na2S2O3和0.1 mol/L H2SO4溶液各5 mL,加水5 mL,反应温度10℃ |
| B、0.1 mol/L Na2S2O3和0.1 mol/L H2SO4溶液各5 mL,加水10 mL,反应温度10℃ |
| C、0.1 mol/L Na2S2O3和0.1 mol/L H2SO4溶液各5 mL,加水10 mL,反应温度30℃ |
| D、0.2 mol/L Na2S2O3和0.1 mol/L H2SO4溶液各5 mL,加水10 mL,反应温度30℃ |
将一定量MnO2和KClO3混合加热,反应完全后,将剩余固体与过量的浓盐酸混合加热,待反应完毕后,将溶液蒸干,所得固体与原混合物质量相等,则原混合物中KClO3的质量分数约为( )
| A、87% | B、53% |
| C、47% | D、58% |
金属、金属材料的性质在很大程度上决定了它们的用途.下列相关说法中不正确的是( )
| A、钛合金与人体具有很好的“相容性”,可以用来制造人造骨骼 |
| B、铁具有良好的导热性,可以用于制造炊具 |
| C、不锈钢抗腐蚀性好,常用于制造医疗器械 |
| D、铅锑合金的熔点较低、电阻率较大,常用于制成发热体 |
吸热反应一定是( )
| A、释放能量 |
| B、储存能量 |
| C、需要加热才能发生 |
| D、反应物总能量高于生成物总能量 |
已知15g化合物A完全氧化,把产物通过浓硫酸和碱石灰,浓硫酸增重9g,碱石灰增重39.6g,用现代物理方法测定:①该有机物的质谱图如图所示 ②核磁共振仪1,3,5测出A的核磁共振氢谱有5个峰,其面积之比为1:2:2:2:3.

则下列说法正确的是( )

则下列说法正确的是( )
| A、该有机物的分子式为C9H10O |
| B、该有机物的摩尔质量为150 |
C、该物质的结构简式可能为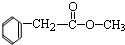 |
| D、该有机物一定不能与Na2CO3反应 |
造成世界有名的“八大公害”事件中,污染事件发生最多的是( )
| A、水污染 | B、食品污染 |
| C、大气污染 | D、重金属污染 |
某无色溶液中放人铝片后有氢气产生,则下列离子在该溶液中肯定可以大量存在的是( )
| A、Na+ |
| B、Mg2+ |
| C、OH- |
| D、HCO3- |
下列说法正确的是( )
| A、检测乙醇中是否含有水可加入少量的无水硫酸铜,如变蓝则含水 |
| B、除去乙醇中的微量水可加入金属钠,使其完全反应 |
| C、获得无水乙醇的方法通常采用先用浓H2SO4吸水,然后再加热蒸馏的方法 |
| D、获得无水乙醇的方法通常采用先用生石灰吸水,然后再加热蒸馏的方法 |