题目内容
若NA代表阿伏加德罗常数的值,则下列叙述中,正确的是( )
| A、一定条件下,足量铜与200 g 98%的浓硫酸充分反应,转移电子数目为2NA | ||
| B、16 g氧气和臭氧的混合气体中含有的氧原子数为NA | ||
C、1 L 0.5 mol?L-1 Na2CO3溶液中含有的CO
| ||
| D、78 g Na2O2中所含阴离子的数目是NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、铜与稀硫酸不反应;
B、根据氧气和臭氧均由氧原子构成来分析;
C、CO
是弱酸根会水解被消耗;
D、根据n=
并结合Na2O2中含2个Na+和1个O22-来分析.
B、根据氧气和臭氧均由氧原子构成来分析;
C、CO
2- 3 |
D、根据n=
| m |
| M |
解答:
解:A、一旦浓硫酸变稀后,铜与稀硫酸不反应,故无法计算出反应掉的硫酸,即无法计算醋转移电子的数目,故A错误;
B、氧气和臭氧均由氧原子构成,而16 g氧气和臭氧的混合气体中含有的氧原子的物质的量n=
=
=1mol,个数为NA个,故B正确;
C、CO
是弱酸根会水解被消耗,故C错误;
D、Na2O2的物质的量n=
=
=1mol,而1molNa2O2中含1molO22-,个数为NA个,故D正确.
故选BD.
B、氧气和臭氧均由氧原子构成,而16 g氧气和臭氧的混合气体中含有的氧原子的物质的量n=
| m |
| M |
| 16g |
| 16g/mol |
C、CO
2- 3 |
D、Na2O2的物质的量n=
| m |
| M |
| 78g |
| 78g/mol |
故选BD.
点评:本题考查了阿伏伽德罗常数的有关计算,掌握公式的运用以及物质的结构是解题关键,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
用NA表示阿伏加德罗常数,下列说法中正确的是( )
①18g D2O含有的电子数为10NA
②同温、同压下,相同体积的氟气和氩气所含的原子数相等
③标准状况下,11.2L以任意比例混合的氮气和氧气所含的原子数为NA
④在标准状况下,22.4LSO3的物质的量为1mol
⑤等物质的量的Na2O和Na2O2中含有的阴离子总数相等
⑥0.1molOH-含0.1NA个电子
⑦1mol Na2O2与水完全反应时转移电子数为2NA.
①18g D2O含有的电子数为10NA
②同温、同压下,相同体积的氟气和氩气所含的原子数相等
③标准状况下,11.2L以任意比例混合的氮气和氧气所含的原子数为NA
④在标准状况下,22.4LSO3的物质的量为1mol
⑤等物质的量的Na2O和Na2O2中含有的阴离子总数相等
⑥0.1molOH-含0.1NA个电子
⑦1mol Na2O2与水完全反应时转移电子数为2NA.
| A、③⑤⑥⑦ | B、③⑤ |
| C、①②④⑦ | D、③④⑤⑥ |
已知15g化合物A完全氧化,把产物通过浓硫酸和碱石灰,浓硫酸增重9g,碱石灰增重39.6g,用现代物理方法测定:①该有机物的质谱图如图所示 ②核磁共振仪1,3,5测出A的核磁共振氢谱有5个峰,其面积之比为1:2:2:2:3.

则下列说法正确的是( )

则下列说法正确的是( )
| A、该有机物的分子式为C9H10O |
| B、该有机物的摩尔质量为150 |
C、该物质的结构简式可能为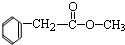 |
| D、该有机物一定不能与Na2CO3反应 |
下列分散系与纳米级微粒在直径上具有相同数量级的是( )
| A、溶液 | B、胶体 |
| C、悬浊液 | D、乳浊液 |
某学生用NaHCO3和KHCO3组成的某混合物进行实验,测得如下数据(盐酸的物质的量浓度相等),下列分析推理正确的是( )
| 50mL盐酸 | 50mL盐酸 | 50mL盐酸 | |
| m(混合物) | 9.2g | 15.7g | 27.6g |
| VCO2(标况) | 2.24L | 3.36L | 3.36L |
| A、盐酸的物质的量浓度为3.0mol/L |
| B、根据表中数据不能计算出混合物中NaHCO3的质量分数 |
| C、向50mL盐酸中加入混合物27.6g时,盐酸过量 |
| D、15.7g混合物能恰好与盐酸完全反应 |
物质的量相同的镁和铝,跟足量的盐酸反应,失去电子数之比为( )
| A、1:1 | B、2:3 |
| C、24:27 | D、3:4 |
以下是某学生的实验操作,正确的是( )
| A、稀释浓硫酸时,先在烧杯中加入一定体积的浓硫酸,后注入蒸馏水 |
| B、用蒸馏分离苯和溴苯 |
| C、用裂化汽油萃取溴水中的溴 |
| D、用酒精萃取碘水中的碘 |
