同体积同物质的量浓度的稀H2SO4与NaOH溶液混合后,滴入紫色石蕊试剂后溶液呈( )
| A、红色 | B、紫色 | C、蓝色 | D、无色 |
下列离子方程式书写不 正确的是( )
| A、盐酸与Na2SiO3溶液混合:SiO32-+2H+═H2SiO3↓ | ||||
| B、往澄清石灰水中通入过量SO2:SO2+Ca2++2OH-═CaSO3↓+H2O | ||||
| C、NO2通入水中:H2O+3NO2═2H++2NO3-+NO | ||||
D、浓盐酸和二氧化锰共热制取Cl2:MnO2+4H++2Cl-
|
下列各组离子中,在碱性溶液中能大量共存,且溶液为无色透明的是( )
| A、K+、MnO4-、SO42-、Cl- |
| B、Ca2+、HCO3-、NO、SO42- |
| C、Na+、AlO2-、NO3-、CO32- |
| D、NH4+、SO42-、S2-、Cl- |
T℃时,A气体与B气体反应生成C气体,反应过程中A、B、C浓度变化如图(Ⅰ).若保持其他条件不变,温度分别为T1和T2时,B的体积分数与时间的关系如图(Ⅱ),则下列结论正确的是( )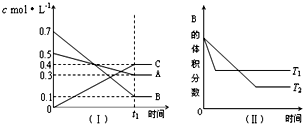

| A、在(t1+10)min时,保持其他条件不变,增大压强,平衡向逆反应方向移动 |
| B、(t1+10)min时,保持容器体积不变,通入稀有气体,平衡向逆反应方向移动 |
| C、其他条件不变,升高温度,正、逆反应速率均增大,且A的转化率减小 |
| D、T℃时,在相同容器中,若由0.4mo1?L-1 A、0.4mo1?L-1 B和0.2mo1?L-1 C反应,达到平衡后,C的浓度为0.4mo1?L-1 |
从物质的量浓度为1mol?L-1的氢氧化钠溶液1L中取出100mL.下面关于这100mL溶液的叙述中不正确的是( )
| A、物质的量浓度为0.1mol?L-1 |
| B、物质的量浓度为1mol?L-1 |
| C、含氢氧化钠4g |
| D、含氢氧化钠0.1mol |
甲烷中的碳原子是sp3杂化,下列用*表示碳原子的杂化和甲烷中的碳原子杂化状态一致的是( )
| A、CH3-C*H2-CH3 |
| B、C*H2=CH-CH3 |
| C、CH2=C*H-CH3 |
| D、CH2=CH-C*H3 |
下列叙述中错误的是( )
| A、水玻璃和石英的主要成份都是SiO2 |
| B、Al和Cu都是用还原法从它们的矿石中冶炼出来 |
| C、氧化铝陶瓷和氮化硅陶瓷都属于高温结构陶瓷 |
| D、常温下浓硫酸和浓硝酸都可贮存在铁制容器中 |
1体积某气态烃A最多和2体积氯化氢加成生成氯代烷烃,1mol此氯代烷烃能和6molCl2发生取代反应,生成物中只有碳、氯两种元素,则A的化学式( )
| A、C3H4 |
| B、C2H4 |
| C、C4H6 |
| D、C2H2 |
设NA为阿伏加德罗常数,下列叙述中正确的是( )
| A、46 g NO2 和 N2O4混合气体中含有原子总数为3NA |
| B、标准状况下22.4L H2中含原子数为NA |
| C、7.1g氯气与足量NaOH溶液反应转移的电子数为0.2NA |
| D、1mol Fe与足量的稀HNO3反应,转移2NA个电子 |