题目内容
从物质的量浓度为1mol?L-1的氢氧化钠溶液1L中取出100mL.下面关于这100mL溶液的叙述中不正确的是( )
| A、物质的量浓度为0.1mol?L-1 |
| B、物质的量浓度为1mol?L-1 |
| C、含氢氧化钠4g |
| D、含氢氧化钠0.1mol |
考点:物质的量浓度
专题:物质的量浓度和溶解度专题
分析:溶液具有均一稳定性
A、根据溶液的物质的量浓度与体积无关;
B、根据溶液的物质的量浓度与体积无关;
C、根据m=cvM来计算;
D、根据n=cv来计算;
A、根据溶液的物质的量浓度与体积无关;
B、根据溶液的物质的量浓度与体积无关;
C、根据m=cvM来计算;
D、根据n=cv来计算;
解答:
解:A、因溶液的物质的量浓度与体积无关,所以这200mL溶液的浓度仍然为1mol/L,故A错误;
B、因溶液的物质的量浓度与体积无关,所以这200mL溶液的浓度仍然为1mol/L,故B正确;
C、因m=cvM=1mol/L×0.1L×40g/mol=4g,故C正确;
D、因n=cv=1mol/L×0.1L=0.1mol,故D正确;
故选A.
B、因溶液的物质的量浓度与体积无关,所以这200mL溶液的浓度仍然为1mol/L,故B正确;
C、因m=cvM=1mol/L×0.1L×40g/mol=4g,故C正确;
D、因n=cv=1mol/L×0.1L=0.1mol,故D正确;
故选A.
点评:本题主要考查了物质的量浓度的有关计算,难度不大,需要注意的是溶液的物质的量浓度与体积无关.

练习册系列答案
 高效智能课时作业系列答案
高效智能课时作业系列答案 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案
相关题目
下列说法正确的是( )
| A、需要加热的化学反应都是吸热反应 |
| B、应用盖斯定律可以计算某些难以测量的反应焓变 |
| C、任何能使熵值增大的过程都能自发进行 |
| D、化学平衡发生移动,平衡常数一定发生变化 |
下列各组离子,在水溶液中能大量共存的是( )
| A、Al3+、Ag+、NO3-、Cl- |
| B、Fe2+、H+、NO3-、Cl- |
| C、K+、NO3-、S2-、OH- |
| D、K+、H+、Cl-、AlO2- |
下列操作中,溶液的颜色不发生变化的是( )
| A、氯化铁溶液中加入足量铁粉,充分振荡 |
| B、氯化铁溶液中滴加硫氰化钾(KSCN)溶液 |
| C、氧化铜固体加入稀盐酸中,完全溶解 |
| D、碳酸氢钠溶液中滴加稀盐酸 |
用NA表示阿伏加德罗常数,下列说法正确的是( )
| A、常温常压下,1 mol甲基(-CH3)所含的电子数为9NA |
| B、9 g重水所含有的电子数为5NA |
| C、标准状况下,11.2 L氯仿中含有的C-Cl键的数目为1.5NA |
| D、1molCl2参加反应,转移电子数一定为2NA个 |
下列分散系属于胶体的是( )
| A、淀粉溶液 | B、食盐水 |
| C、牛奶 | D、碘酒 |
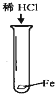
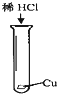
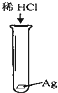
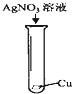
 某同学设计如图所示装置分别进行探究实验(夹持装置已略去),请回答下列问题:
某同学设计如图所示装置分别进行探究实验(夹持装置已略去),请回答下列问题: