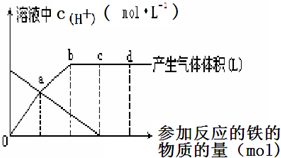
 铁与HNO3作用时,还原产物除与HNO3浓度有关外,还与温度有关.已知在与冷稀HNO3反应时,主要还原产物为NO气体;在与热的稀HNO3作用时,主要还原产物为N2O气体;当HNO3更稀时,其重要还原产物是NH4+.现有铁与稀HNO3的反应变化如图所示,假设曲线的各段内只有一种还原产物,且生成该还原产物的反应已全部完成,下列叙述正确的是( )
铁与HNO3作用时,还原产物除与HNO3浓度有关外,还与温度有关.已知在与冷稀HNO3反应时,主要还原产物为NO气体;在与热的稀HNO3作用时,主要还原产物为N2O气体;当HNO3更稀时,其重要还原产物是NH4+.现有铁与稀HNO3的反应变化如图所示,假设曲线的各段内只有一种还原产物,且生成该还原产物的反应已全部完成,下列叙述正确的是( )| A、0点到a点的还原产物是NO |
| B、因反应放热,使溶液温度升高,a点到b点的还原产物是N2O |
| C、反应过程到达b点时HNO3已完全反应 |
| D、c点和d点参加反应的铁的物质的量之比是2:3 |
下列反应的现象描述与离子方程式都正确的是( )
| A、碳酸钙固体中加入盐酸,固体溶解,有气泡逸出; CO32-+2H+=H2O+CO2↑ |
| B、氯化铁溶液中加入过量铁粉,振荡,充分反应后溶液变红色; Fe+2Fe3+=3Fe2+ |
| C、将金属镁投入稀盐酸中,有无色气泡产生; Mg+2H++2Cl-=MgCl2+H2↑ |
| D、氢氧化钡溶液中滴加稀硫酸,有白色沉淀产生;Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O |
有 ①Na2CO3溶液 ②CH3COONa溶液 ③NaOH溶液各25mL,物质的量浓度均为0.1mol?L-1,下列说法正确的是( )
| A、3种溶液pH的大小顺序是②>①>③ |
| B、若向3种溶液都通入足量二氧化碳,pH变化最大的是③ |
| C、若分别加入25mL0.1mol?L-1盐酸后,pH最小的是③ |
| D、若3种溶液的pH均为9,则物质的量浓度的大小顺序是②>①>③ |
向某无色溶液中逐滴加入稀氨水,开始产生沉淀,继续滴加,沉淀逐渐消失,仍得无色溶液,则原溶液可能是( )
| A、AlCl3 |
| B、FeCl3 |
| C、BaCl2 |
| D、AgNO3 |
下列有关表达正确的是( )
A、热化学方程式C2H2(g)+
| ||
| B、H+(aq)+OH-(aq)=H2O(l);△H=-57.3 kJ/mol,表示含1molNaOH的氢氧化钠溶液与含0.5mol H2SO4的浓硫酸混合后放出57.3 kJ的热量 | ||
| C、少量的钠投入足量的水中:2Na+2H2O═2Na++2OH-+H2↑ | ||
| D、向明矾KAl(SO4)2溶液中滴入氢氧化钡溶液,至SO42-恰好沉淀完全:Al3++2SO42-+2Ba2++3OH-═2BaSO4↓+Al(OH)3↓ |
要将NaCl和CaCl2固体混合物分离,不需采用的操作是( )
| A、溶解 | B、称量 | C、过滤 | D、蒸发 |
可能含有N2、HCl、CO、CO2的混合气体,依次通过足量的碳酸氢钠溶液和灼热的氧化铜,恢复到原来的温度和压强,气体体积没有变化;再通过足量的过氧化钠,气体体积减少;最后通过灼热的铜网,恢复到原来的温度和压强,体积又减少,并有剩余气体.若上述反应均完全,则对混合气体成份的判断正确的是( )
| A、一定有N2和CO2,可能有HCl和CO |
| B、一定有N2,且HCl、CO、CO2中至少含有一种 |
| C、一定有N2、HCl、CO、CO2 |
| D、一定有N2、CO2、CO,一定没有HCl |
设NA为阿伏加德罗常数,下列说法正确的是( )
| A、1 mol Fe和足量Cl2反应转移的电子数为2NA |
| B、标况下,11.2LCH4和C2H4混合气体中含氢原子数为2NA |
| C、标准状况下,22.4 L 氖气中含氖原子数为2NA |
| D、在1L 0.1 mol?L-1Na2SO4溶液中含离子数:Na+ 0.2 NA、SO42- 0.1 NA |
能正确表示下列反应的离子方程式为( )
| A、向碳酸氢镁溶液中滴加少量石灰水:Mg2++2HCO3-+2Ca2++4OH-=Mg(OH)2↓+2CaCO3↓+H2O |
| B、在强碱溶液中,次氯酸钠与氢氧化铁反应生成Na2FeO4:3ClO-+2Fe(OH)3=2FeO42-+3Cl-+H2O+4H+ |
| C、向NaAlO2溶液中通入过量的CO2制取Al(OH)3:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3- |
| D、漂白粉[主要成分Ca(ClO)2,Ca(OH)2]在空气中失效:ClO-+CO2+H2O=HClO+HCO3- |
在20℃时,将一种可溶性盐与一种不溶性物质组成的固体混合物30g,投入40g水中,充分搅拌、溶解、过滤,剩余固体15.6g,此15.6g固体加入40g水中充分搅拌、溶解、过滤,还剩余5g固体,则该可溶性盐在20℃时的溶解度为( )
| A、26.5g |
| B、31.25g |
| C、36.0g |
| D、无法计算 |