下列根据实验现象所得出的结论一定正确的是( )
| A、某无色溶液滴加酚酞试液后显红色,结论:该溶液中一定含OH- |
| B、某无色溶液加入盐酸产生无色无味气体,结论:溶液中一定含有CO32- |
| C、某气体能使品红溶液褪色,结论:该气体为SO2气体 |
| D、向溶液X中先滴加稀硝酸,再滴加Ba(NO3)2溶液,出现白色沉淀,结论:溶液X中一定含有SO42- |
初中化学教材中“家庭小实验”是利用家庭日常生活用品进行化学学习和探究的活动.食盐、食醋、纯碱等均为家庭厨房中常用的物质,利用这些物质你能完成的实验是( )
①检验自来水中是否含氯离子
②鉴别食盐和纯碱
③检验鸡蛋壳能否溶于酸
④除去热水瓶中的水垢.
①检验自来水中是否含氯离子
②鉴别食盐和纯碱
③检验鸡蛋壳能否溶于酸
④除去热水瓶中的水垢.
| A、①②③④ | B、①③ |
| C、②④ | D、②③④ |
下列各组溶液不用其他试剂即能鉴别开的是( )
| A、MgCl2和NaOH |
| B、NaCl和AgNO3 |
| C、Na2CO3和HCl |
| D、AlCl3和KOH |
元素周期表中电负性最大的元素是( )
| A、Fr | B、F | C、H | D、N |
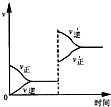 若平衡体系A+B═C+D,增大压强时反应速率变化如图所示.则下列关于各物质状态的说法正确的是( )
若平衡体系A+B═C+D,增大压强时反应速率变化如图所示.则下列关于各物质状态的说法正确的是( )| A、A、B、C、D都是气体 |
| B、C、D都是气体,A、B中有一种是气体 |
| C、A、B都不是气体,C、D中有一种是气体 |
| D、A、B都是气体,C、D中有一种是气体 |
下列反应条件的控制中,不恰当的是( )
| A、为了防止铁生锈,在其表面涂一层防锈油漆 |
| B、为防止火灾,在面粉厂、加油站等场所要严禁烟火 |
| C、为加快KClO3的分解速率,加入MnO2 |
| D、为加快H2O2的分解速率,把反应容器放到冷水中冷却 |
为鉴别K2CO3和NaHCO3两种白色固体,有四名同学分别设计了下列四种不同的方法,其中不可行的是( )
| A、分别滴加0.1 mol?L-1的盐酸,看气泡产生的快慢 |
| B、分别取样在试管中加热,将可能产生的气体通入澄清石灰水,观察有无白色沉淀生成 |
| C、分别取样配成溶液,滴加Ba(OH)2溶液,观察有无白色沉淀 |
| D、分别配成溶液,做焰色反应实验,观察火焰的颜色 |
