下列有关化学实验基本知识和基本操作的描述不正确的是( )
| A、丁达尔效应可以用于区别FeCl3溶液和Fe(OH)3胶体 |
| B、过滤和蒸发操作均用到玻璃棒,但玻璃棒的作用不相同 |
| C、加入盐酸,能产生使澄清石灰水变浑浊的气体,则溶液中一定含有CO32- |
| D、先加入BaCl2溶液,再加入HNO3溶液,产生了白色沉淀,则溶液中一定含有大量的SO42- |
常温下,下列各组物质不能用一种试剂通过化学反应区别的是( )
| A、MnO2CuO FeO |
| B、Na2CO3CaCO3 K2CO3 |
| C、AgNO3KNO3 Na2CO3 |
| D、(NH4)2SO4 K2SO4 NH4Cl |
下列说法正确的是( )
| A、碘是人体必需的微量元素,所以要多吃富含I2的食物 |
| B、金属钠、钾、锂保存在煤油中 |
| C、碳酸钠溶液用带磨口玻璃塞的普通试剂瓶贮存 |
| D、量筒、容量瓶、滴定管上均标有温度 |
下列说法正确的是( )
| A、纤维素和淀粉遇碘水均显蓝色 |
| B、蛋白质、乙酸和葡萄糖均属电解质 |
| C、乙酸乙酯和食用植物油均可水解生成乙醇 |
| D、红外光谱仪、核磁共振仪、质谱仪都可用于有机化合物结构的分析 |
下列装置或操作能达到实验目的是( )
A、 制取Fe(OH)2沉淀 |
B、 检查装置气密性 |
C、 干燥HBr |
D、 检验钾元素的存在 |
下列实验能达到预期目的是( )
①用乙醇和浓硫酸除去乙酸乙酯中的少量乙酸
②将Cl2的制备和性质实验联合进行以减少实验中的空气污染
③用食醋和澄清石灰水验证蛋壳中含有碳酸盐
④将碘水倒入分液漏斗,加适量乙醇,振荡后静置,可将碘萃取到乙醇中
⑤用溴水鉴别直馏汽油和裂化汽油.
①用乙醇和浓硫酸除去乙酸乙酯中的少量乙酸
②将Cl2的制备和性质实验联合进行以减少实验中的空气污染
③用食醋和澄清石灰水验证蛋壳中含有碳酸盐
④将碘水倒入分液漏斗,加适量乙醇,振荡后静置,可将碘萃取到乙醇中
⑤用溴水鉴别直馏汽油和裂化汽油.
| A、①②④ | B、③④⑤ |
| C、②③④ | D、②③⑤ |
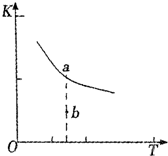 利用催化氧化反应将SO2转化为SO3是工业上生产硫酸的关键步骤.
利用催化氧化反应将SO2转化为SO3是工业上生产硫酸的关键步骤.