对于可逆反应C(s)+H2O(g)?CO(g)+H2(g),在一定温度下达到平衡时,其平衡常数表达式正确的是( )
| A、K=[c(C)?c(H2O)]/[c(CO)?c(H2)] |
| B、K=[c(CO)?c(H2)]/[c(C)?c(H2O)] |
| C、K=[c(CO)?c(H2)/[c(H2O)]] |
| D、K=[c(H2O)]/[c(CO)?c(H2)] |
在一定温度下将CO和水蒸气各1mol放在密闭的容器中反应:CO+H2O?CO2+H2,达到平衡后,测得CO2为0.6mol,再通入4mol水蒸气,达到平衡后CO2的物质的量为( )
| A、等于0.6mol |
| B、等于1mol |
| C、大于0.6mol小于1mol |
| D、大于1mol |
一定条件下,体积为2L的密闭容器中,1mol X和3mol Y进行反应:X(g)+3Y(g)?2Z(g),经12s达到平衡,生成0.6mol Z.下列说法正确的是( )
| A、以X浓度变化表示的反应速率为0.25 mol?L-1?s-1 |
| B、12 s后将容器体积扩大为10 L,Z的平衡浓度变为原来的1/5 |
| C、若增大X的浓度,则物质Y的转化率减小 |
| D、若该反应的△H<0,升高温度,平衡常数K减小 |
采用NH3作还原剂,除去烟气中的氮氧化物,反应原理为:NO(g)+NO2(g)+2NH3(g)?2N2(g)+3H2O(g).如图是烟气以固定的流速通过两种不同催化剂①和②时,测量相同时间得到的烟气脱氮率图象.根据该图象,下列说法中正确的是( )
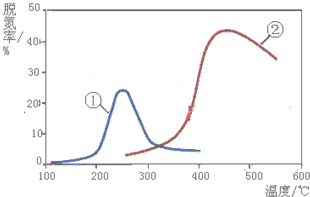

| A、上述反应的正反应为吸热反应 |
| B、催化剂①、②分别适合于250℃和450℃左右脱氮 |
| C、催化剂②比①脱氮效果好,说明催化剂②能导致该反应平衡向右移动程度更大 |
| D、相同条件下,改变压强对脱氮率没有影响 |
对可逆反应2A(s)+3B(g)?C(g)+2D(g);△H<0,在一定条件下达到平衡,下列有关叙述正确的是( )
| A、增加A的量,平衡向正反应方向移动 |
| B、增大B的浓度,v(正)>v(逆) |
| C、压强增大一倍(压缩体积),平衡不移动,v(正)、v(逆)不变 |
| D、升高温度,平衡向逆反应方向移动,v(逆)增大、v(正)减小 |
XSO4溶液与NaOH溶液反应,可生成X3(OH)4SO4沉淀和Na2SO4溶液,现有V1mL0.1mol/L XSO4溶液和V2mL 0.2mol/L NaOH溶液(V1+V2=50),为了使沉淀的质量达到最大值,V1和V2的取值应为( )
| A、V1=30,V2=20 |
| B、V1=20,V2=30 |
| C、V1=10,V2=40 |
| D、V1=15,V2=35 |
如图有关电化学的示意图正确的是( )
A、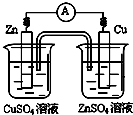 |
B、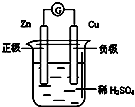 |
C、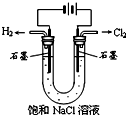 |
D、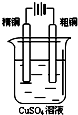 |