关于氢键,下列说法正确的是( )
| A、含氢元素的化合物中一定有氢键 |
B、因为分子间存在氢键的缘故,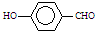 比 比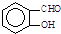 熔沸点高 熔沸点高 |
| C、由于氢键比范德华力强,所以H2O分子比H2S分子稳定 |
| D、“可燃冰”--甲烷水合物(例如:8CH4?46H2O)中CH4与H2O之间存在氢键 |
下列说法正确的是( )
| A、HF、HCl、HBr、HI的热稳定性依次减弱,沸点却依次升高 |
| B、熔融状态下能导电的化合物一定含离子键;金属与非金属元素形成的化合物一定是离子化合物 |
| C、NCl3分子中所有的原子均为8电子稳定结构 |
| D、NaHSO4晶体中阴、阳离子的个数是1:2且熔化时破坏的是离子键和共价键 |
在密闭容器中进行可逆反应,A与B反应生成C,其反应速率分别用VA、VB、V C〔mol/(L?s)〕表示,且VA、VB、VC之间有以下关系:VB=3VA,VC=2VA,3VC=2VB,则此反应表示为( )
| A、A(g)+B(g)?C(g) |
| B、2A(g)+2B(g)?3C(g) |
| C、3A(g)+B(g)?2C(g) |
| D、A(g)+3B(g)?2C(g) |
根据下列反应判断还原剂的还原性由强到弱的顺序,正确的是( )
①Cl2+2KI═I2+2KCl
②2FeCl3+2HI═I2+2FeCl2+2HCl
③2FeCl2+Cl2═2FeCl3
④I2+SO2+2H2O═2HI+H2SO4.
①Cl2+2KI═I2+2KCl
②2FeCl3+2HI═I2+2FeCl2+2HCl
③2FeCl2+Cl2═2FeCl3
④I2+SO2+2H2O═2HI+H2SO4.
| A、SO2>I->Fe2+>Cl- |
| B、Cl2>Fe3+>I2>SO2 |
| C、Fe2+>Cl->I->SO2 |
| D、Cl->Fe2+>I->SO2 |
在298K时,NaCl 在水中的溶解度为
水.如将1molNaCl溶解在1L水中,此溶解过程中体系的△H-T△S和熵如何变化( )
| 26g |
| 100g |
| A、△H-T△S<0△S<0 |
| B、△H-T△S<0△S>0 |
| C、△H-T△S>0△S>0 |
| D、△H-T△S>0△S<0 |
下列反应不属于可逆反应的是( )
| A、氯气溶于水 | |||
| B、氨气溶于水 | |||
C、可充电电池的反应如2Ag+Zn(OH)2
| |||
| D、工业合成氨 |
在密闭容器中进行如下反应:X2(气)+Y2(气)?2Z(气),已知 X2、Y2、Z的起始浓度分别为 0.1mol/L,0.3mol/L,0.2mol/L,在一定的条件下,当反应达到平衡时,各物质的浓度有可能是( )
| A、Y2为0.2 mol/L |
| B、Y2 为0.35 mol/L |
| C、X2 为0.2 mol/L |
| D、Z为 0.4 mol/L |
一定能使反应速率加快的因素是( )
①扩大容器的容积 ②增大压强 ③增加反应物的质量 ④升高温度 ⑤缩小容积.
①扩大容器的容积 ②增大压强 ③增加反应物的质量 ④升高温度 ⑤缩小容积.
| A、③④ | B、②③④ |
| C、②③④⑤ | D、④ |
对电解质的叙述正确的是( )
| A、溶于水后得到的溶液能导电的物质 |
| B、NaCl溶液在电流作用下电离成Na+和Cl- |
| C、KNO3是电解质故KNO3晶体能导电 |
| D、二氧化碳的水溶液能导电,但二氧化碳不是电解质 |