下列离子方程式,一定正确的是( )?
| A、亚硫酸钠与稀硝酸反应SO32-+2H+=SO2↑+H2O?? |
| B、氢氧化钡中加入稀硫酸:H++OH-=H2O |
| C、用碳酸钠溶液吸收少量二氧化硫:2CO32-+SO2+H2O=2HCO3-+SO32- |
| D、将少量SO2气体通入Ca(ClO)2溶液中?SO2+Ca2++2ClO-+H2O=CaSO3↓+2HClO |
下列有关物质性质的比较顺序中,不正确的是( )
| A、热稳定性:HF>HCl>HBr>HI |
| B、微粒半径:K+>Na+>Mg2+>Al3+ |
| C、酸性:HClO4>H2SO4>H3PO4>H2SiO3 |
| D、沸点:HF>HCl>HBr>HI |
下列离子方程式的书写正确的是( )
| A、NaHSO4与NaOH溶液反应:HSO4-+OH-=SO42-+H2O |
| B、Fe与盐酸的反应放出H2:Fe+H+=Fe2++H2↑ |
| C、大理石与盐酸反应放出CO2气体:CO32-+2H+=CO2+H2O |
| D、醋酸与烧碱溶液混合:CH3COOH+OH-=CH3COO-+H2O |
下列元素中,原子半径最小的是( )
| A、I | B、Br | C、Cl | D、F |
按照原子核外电子排布规律:各电子层最多容纳的电子数为2n2(n为电子层数,其中,最外层电子数不超过8个,次外层不超过18个).1999年已发现了核电荷数为118的元素,其原子核外电子层排布是( )
| A、2,8,18,32,32,18,8 |
| B、2,8,18,32,50,8 |
| C、2,8,18,32,18,8 |
| D、2,8,18,32,50,18,8 |
下列物质性质的变化规律与分子间作用力有关的是( )
| A、金刚石硬度大于硅,其熔点也高于硅 |
| B、HF、HCl、HBr、HI热稳定性依次减弱 |
| C、NaF、NaCl、NaBr、NaI的熔点依次降低 |
| D、F2、Cl2、Br2、I2的熔、沸点逐渐升高 |
碳原子的最外电子层的各轨道中,基态时电子通常排布方式是( )
A、 |
B、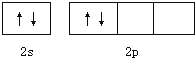 |
C、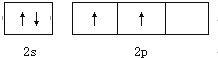 |
D、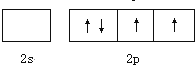 |
 科学研究发现铂的两种化合物(短线表示化学健)有不同的特性,其中a具有抗癌作用,而b没有;则下列正确的说法是( )
科学研究发现铂的两种化合物(短线表示化学健)有不同的特性,其中a具有抗癌作用,而b没有;则下列正确的说法是( )| A、a、b分子中,Pt原子与2个Cl原子,2个N原子间形成的结构与CH2Cl2相似 |
| B、a在水中的溶解度比b在水中的溶解度大 |
| C、a、b互为同素异形体 |
| D、a、b是同一物质 |
下列各分子中,所有原子都满足最外层为8电子结构的是( )
| A、H2O |
| B、PCl5 |
| C、Cl2 |
| D、BF3 |