题目内容
下列离子方程式,一定正确的是( )?
| A、亚硫酸钠与稀硝酸反应SO32-+2H+=SO2↑+H2O?? |
| B、氢氧化钡中加入稀硫酸:H++OH-=H2O |
| C、用碳酸钠溶液吸收少量二氧化硫:2CO32-+SO2+H2O=2HCO3-+SO32- |
| D、将少量SO2气体通入Ca(ClO)2溶液中?SO2+Ca2++2ClO-+H2O=CaSO3↓+2HClO |
考点:离子方程式的书写
专题:离子反应专题
分析:A.发生氧化还原反应生成硫酸根离子、NO和水;
B.漏写生成硫酸钡的离子反应;
C.反应生成碳酸氢钠和亚硫酸钠;
D.发生氧化还原反应生成硫酸钙.
B.漏写生成硫酸钡的离子反应;
C.反应生成碳酸氢钠和亚硫酸钠;
D.发生氧化还原反应生成硫酸钙.
解答:
解:A.亚硫酸钠与稀硝酸反应的离子反应为2NO3-+3SO32-+2H+=2NO↑+H2O+3SO42-,故A错误;
B.氢氧化钡中加入稀硫酸的离子反应为SO42-+Ba2++2H++2OH-=2H2O+BaSO4↓,故B错误;
C.用碳酸钠溶液吸收少量二氧化硫的离子反应为2CO32-+SO2+H2O=2HCO3-+SO32-,故C正确;
D.将少量SO2气体通入Ca(ClO)2溶液中的离子反应为SO2+Ca2++ClO-+H2O=CaSO4↓+2H++Cl-,故D错误;
故选C.
B.氢氧化钡中加入稀硫酸的离子反应为SO42-+Ba2++2H++2OH-=2H2O+BaSO4↓,故B错误;
C.用碳酸钠溶液吸收少量二氧化硫的离子反应为2CO32-+SO2+H2O=2HCO3-+SO32-,故C正确;
D.将少量SO2气体通入Ca(ClO)2溶液中的离子反应为SO2+Ca2++ClO-+H2O=CaSO4↓+2H++Cl-,故D错误;
故选C.
点评:本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重复分解反应、氧化还原反应的离子反应考查,题目难度不大.

练习册系列答案
相关题目
分子中具有手性碳原子的是 ( )
| A、甘油 |
| B、3-甲基己烷 |
| C、2-甲基-1-丁烯 |
| D、2,2-二甲基丙烷 |
菜在生长的过程中,常喷洒农药防治虫害.据有关专家介绍,用碱性溶液或清水浸泡,
可使残留在蔬菜上的农药的毒性降低.因此,买来的蔬菜在食用之前最好用稀碱水或清水浸泡一段时间,浸泡蔬菜时可加入适量( )
可使残留在蔬菜上的农药的毒性降低.因此,买来的蔬菜在食用之前最好用稀碱水或清水浸泡一段时间,浸泡蔬菜时可加入适量( )
| A、纯碱 | B、白酒 | C、白糖 | D、食醋 |
甲、乙两元素原子的L层电子数都是其他层电子总数的2倍,甲元素原子序数大于乙.下列推断正确的是( )
| A、甲与乙处于同一周期 |
| B、甲与乙处于同一主族 |
| C、甲原子的半径小于乙原子 |
| D、甲与乙的原子序数之和为偶数 |
按照原子核外电子排布规律:各电子层最多容纳的电子数为2n2(n为电子层数,其中,最外层电子数不超过8个,次外层不超过18个).1999年已发现了核电荷数为118的元素,其原子核外电子层排布是( )
| A、2,8,18,32,32,18,8 |
| B、2,8,18,32,50,8 |
| C、2,8,18,32,18,8 |
| D、2,8,18,32,50,18,8 |
下列物质中有4种化学环境不同的氢的是( )
A、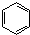 |
B、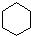 |
C、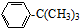 |
| D、CH3CH2CH(CH2CH3)2 |
下列离子方程式书写正确的是( )
| A、向明矾溶液加入过量氨水:Al3++4OH-═〔Al(OH)4〕- |
| B、碳酸钙溶于稀盐酸:CO32-+2H+═H2O+CO2↑ |
| C、SO2通入足量的Ba(NO3)2稀溶液中:3SO2+2H2O+2NO3-+3Ba2+═3BaSO4↓+2NO+4H+ |
| D、一小块钠投入到CuSO4溶液中:2Na+Cu2+═Cu+2Na+ |
将同温同压下的NO、NO2、O2三种气体按以下体积比混合后通入水中,气体不能完全溶于水的是( )
| A、1:2:1 |
| B、1:1:1 |
| C、5:1:4 |
| D、6:2:5 |
下列物质中属于非电解质的是( )
| A、NaOH |
| B、O2 |
| C、Na2CO3 |
| D、蔗糖 |