题目内容
下列有关物质性质的比较顺序中,不正确的是( )
| A、热稳定性:HF>HCl>HBr>HI |
| B、微粒半径:K+>Na+>Mg2+>Al3+ |
| C、酸性:HClO4>H2SO4>H3PO4>H2SiO3 |
| D、沸点:HF>HCl>HBr>HI |
考点:非金属在元素周期表中的位置及其性质递变的规律,微粒半径大小的比较
专题:元素周期律与元素周期表专题
分析:A.非金属性越强,气态氢化物越稳定;
B.具有相同电子排布的离子,原子序数大的离子半径小;
C.元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强;
D.不含氢键的氢化物,相对分子质量越大,沸点越高.
B.具有相同电子排布的离子,原子序数大的离子半径小;
C.元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强;
D.不含氢键的氢化物,相对分子质量越大,沸点越高.
解答:
解:A.非金属性F>Cl>Br>I,气态氢化物的稳定性为HF>HCl>HBr>HI,故A正确;
B.K+核外有3个电子层,离子半径最大,Na+、Mg2+、Al3+离子核外电子排布相同,都有2个电子层,根据离子核电核数越大,半径越小可知Na+>Mg2+>Al3+,则有K+>Na+>Mg2+>Al3+,故B正确;
C.已知非金属性:Cl>S>P>Si,元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强,则有酸性:HClO4>H2SO4>H3PO4>H2SiO3,故C正确;
D.HF含有氢键,沸点最高,而HCl、HBr和HI不含氢键,相对分子质量越大,沸点越高,应为HF>HI>HBr>HCl,故D错误.
故选D.
B.K+核外有3个电子层,离子半径最大,Na+、Mg2+、Al3+离子核外电子排布相同,都有2个电子层,根据离子核电核数越大,半径越小可知Na+>Mg2+>Al3+,则有K+>Na+>Mg2+>Al3+,故B正确;
C.已知非金属性:Cl>S>P>Si,元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强,则有酸性:HClO4>H2SO4>H3PO4>H2SiO3,故C正确;
D.HF含有氢键,沸点最高,而HCl、HBr和HI不含氢键,相对分子质量越大,沸点越高,应为HF>HI>HBr>HCl,故D错误.
故选D.
点评:本题考查非金属性的比较,为高频考点,把握非金属性与微粒还原性、半径、物质酸性和稳定性的关系为解答的关键,侧重规律性知识的考查,注意元素周期表和周期律的应用,选项D为解答的难点,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列实验事实不能证明醋酸是弱酸的是( )
| A、常温下,含有石蕊的醋酸溶液加热颜色变深 |
| B、常温下,测得0.1 mol/L醋酸溶液的pH=4 |
| C、常温下,将pH=1的醋酸溶液稀释1 000倍,测得pH<4 |
| D、常温下,将物质的量浓度相同的醋酸溶液与氢氧化钠溶液等体积混合后恰好中和 |
“84”消毒液的有效成分是NaClO,可使用它进行杀菌消毒.下列说法不正确的是( )
| A、“84”消毒液的消毒原理是它具有较强的碱性 |
| B、臭氧、双氧水、次氯酸等消毒原理是它们具有较强的氧化性 |
| C、酒精消毒的原理是利用变性作用 |
| D、“84”消毒液的消毒原理是它具有较强的氧化性 |
常温下用pH试纸测定某溶液的pH,如果将pH试纸用蒸馏水润湿后,再把待测液滴到pH试纸上,跟比色卡对照,测得pH=6.则此溶液的实际pH( )
| A、大于6 | B、小于6 |
| C、等于6 | D、大于7 |
碳原子的最外电子层的各轨道中,基态时电子通常排布方式是( )
A、 |
B、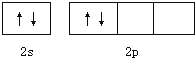 |
C、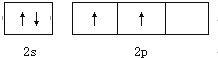 |
D、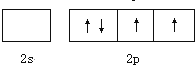 |
下列方程式中,不能用Ba2++SO42-=BaSO4↓来表示的是( )
| A、Ba(NO3)2+H2SO4═Ba2SO4↓+2HNO3 |
| B、BaCl2+Na2SO4═Ba2SO4↓+NaCl |
| C、BaCO3+H2SO4═Ba2SO4↓+H2O+CO2 |
| D、BaCl2+H2SO4═Ba2SO4↓+2HCl |
下列离子方程式书写正确的是( )
| A、硫酸与氢氧化钡反应:Ba2++SO42-=BaSO4↓ |
| B、氧化铜与盐酸反应:O2-+2 H+=H2O |
| C、钠与水反应:Na+2H2O=Na++2 OH-+H2↑ |
| D、澄清石灰水中通入少量二氧化碳:Ca2++2OH-+CO2=CaCO3↓+H2O |
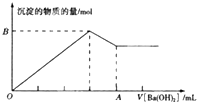 已知Ba[Al(OH)4]2可溶于水,图中表示的向100mL0.02mol.L-1KAl(SO4)2溶液中逐加入0.05mol.L-1Ba(OH)2溶液时(25℃),生成沉淀的物质的量与加入Ba(OH)2溶液的体积的关系.下列说法不正确的是( )
已知Ba[Al(OH)4]2可溶于水,图中表示的向100mL0.02mol.L-1KAl(SO4)2溶液中逐加入0.05mol.L-1Ba(OH)2溶液时(25℃),生成沉淀的物质的量与加入Ba(OH)2溶液的体积的关系.下列说法不正确的是( )| A、所价的Ba(OH)2溶液的c(OH-)=0.1mol.L- |
| B、A点的值是80mL |
| C、B点的值是0.005mol |
| D、当V[Ba(OH)2]时,生成沉淀的质量是0.699g |
列有关物质用途的说法中,正确的是( )
| A、硅可用作绝缘材料 |
| B、液氨可用作制冷剂 |
| C、氯化钠常用于中和胃酸 |
| D、铝制容器常用于盛装稀硫酸 |