下列说法正确的是( )
| A、电子的运动与行星相似,围绕原子核在固定的轨道上高速旋转 |
| B、能量低的电子只能在s轨道上运动,能量高的电子总是在f轨道上运动 |
| C、能层序数越大,s原子轨道的半径越大 |
| D、某微粒的最外层电子排布为2s22p6,则该微粒为Ne |
已知含氧酸可用通式XOm(OH)n表示,如X是S,m=2,n=2,则这个式子表示为H2SO4.一般而言,该式中m 大的是强酸,m小的是弱酸.下列各含氧酸中酸性最强的是( )
| A、HClO3 |
| B、H2SeO3 |
| C、H2BO2 |
| D、HMnO4 |
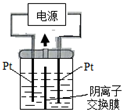 电解装置如图所示,电解槽内装有KI及淀粉溶液,中间用阴离子交换膜隔开.在一定的电压下通电,发现左侧溶液变蓝色,一段时间后,蓝色逐渐变浅.已知:3I2+6OH-═IO3-+5I-+3H2O,下列说法不正确的是( )
电解装置如图所示,电解槽内装有KI及淀粉溶液,中间用阴离子交换膜隔开.在一定的电压下通电,发现左侧溶液变蓝色,一段时间后,蓝色逐渐变浅.已知:3I2+6OH-═IO3-+5I-+3H2O,下列说法不正确的是( )| A、右侧发生的电极方程式:2H2O+2e-═H2↑+2OH- |
| B、电解结束时,右侧溶液中含有IO3- |
| C、电解槽内发生反应的总化学方程式KI+3H2O═KIO3+3H2 |
| D、如果用阳离子交换膜代替阴离子交换膜,电解槽内发生的总化学方程式不变 |
下列由相关实验现象所推出的结论正确的是( )
| A、向氯水中加入有色布条,片刻后有色布条褪色,说明有Cl2存在 |
| B、向溶液中滴加酸化的Ba(NO3)2溶液出现白色沉淀,说明该溶液中一定有SO42- |
| C、Fe与稀HNO3、稀H2SO4反应均有气泡产生,说明Fe与两种酸均发生置换反应 |
| D、分别充满HCl、NH3的烧瓶倒置于水中后液面均迅速上升,说明二者均易溶于水 |
一定温度下,向2.0L恒容密闭容器中充入1.0mol COCl2,反应COCl2(g)?Cl2(g)+CO(g),经过一段时间达到平衡.反应过程中测定的部分数据见下表:下列说法正确的是( )
| t/s | 0 | 2 | 4 | 6 | 8 |
| n(Cl2)/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
| A、反应在前2 s 的平均速率v(CO)=0.080mol?L-1?s-1 |
| B、保持其他条件不变,升高温度,平衡时c(Cl2)=0.11 mol?L-1,则正反应为放热反应 |
| C、向容器中充入0.9 mol COCl2、0.10 mol Cl2和0.10 mol CO,反应达到平衡前v正>v逆 |
| D、若起始向容器中充入1.0 mol Cl2 和0.9 mol CO,达到平衡时,Cl2的转化率大于80% |
 如图所示,当关闭K时,向A(恒容)中充入1mol X、1mol Y,向B(带有活塞)中充入2mol X、2mol Y,起始时,V(A)=V(B)=aL.在相同温度和催化剂存在的条件下,两容器中各自发生下列反应:2X(g)+2Y(g)?Z(g)+2W(g)△H<0,达到平衡(Ⅰ)时,V(B)=0.8aL.请回答:
如图所示,当关闭K时,向A(恒容)中充入1mol X、1mol Y,向B(带有活塞)中充入2mol X、2mol Y,起始时,V(A)=V(B)=aL.在相同温度和催化剂存在的条件下,两容器中各自发生下列反应:2X(g)+2Y(g)?Z(g)+2W(g)△H<0,达到平衡(Ⅰ)时,V(B)=0.8aL.请回答: