题目内容
已知含氧酸可用通式XOm(OH)n表示,如X是S,m=2,n=2,则这个式子表示为H2SO4.一般而言,该式中m 大的是强酸,m小的是弱酸.下列各含氧酸中酸性最强的是( )
| A、HClO3 |
| B、H2SeO3 |
| C、H2BO2 |
| D、HMnO4 |
考点:物质的结构与性质之间的关系
专题:
分析:含氧酸可用通式XOm(OH)n来表示,式中m大于等于2的是强酸,m为0的是弱酸,据此可知,非羟基氧原子数目越大,酸性越强,将选项中含氧酸改写成XOm(OH)n形式,根据非羟基氧原子数目判断.
解答:
解:含氧酸可用通式XOm(OH)n来表示,式中m大于等于2的是强酸,m为0的是弱酸,据此可知,非羟基氧原子数目越大,酸性越强,
A.HClO3可以改写为ClO2(OH)1,非羟基氧原子数目为2;
B.H2SeO3可以改写为SeO1(OH)2,非羟基氧原子数目为1;
C.H2BO2可以改写为B(OH)2,非羟基氧原子数目为0;
D.HMnO4可以改写为MnO3(OH)1,非羟基氧原子数目为3;
HMnO4中非羟基氧原子数目最多,酸性最强,
故选D.
A.HClO3可以改写为ClO2(OH)1,非羟基氧原子数目为2;
B.H2SeO3可以改写为SeO1(OH)2,非羟基氧原子数目为1;
C.H2BO2可以改写为B(OH)2,非羟基氧原子数目为0;
D.HMnO4可以改写为MnO3(OH)1,非羟基氧原子数目为3;
HMnO4中非羟基氧原子数目最多,酸性最强,
故选D.
点评:本题属于信息给予题,正确理解题中所给信息是解本题关键,根据非羟基氧原子数目多少来确定酸性强弱即可,难度不大.

练习册系列答案
相关题目
下列叙述中,正确的是( )
| A、1mol气体所占的体积约为22.4L,不一定要在标准状况下 |
| B、在标准情况下,1mol四氯化碳的体积约为22.4L |
| C、直径介于1nm-100nm之间的微粒成为胶体 |
| D、淀粉溶胶中含有少量的NaCl,可用适量的硝酸银溶液除去 |
向溶液X中持续通入气体Y,不会产生“浑浊-→澄清”现象的是( )
| A、X:漂白粉溶液Y:二氧化硫 |
| B、X:硝酸银溶液Y:氨气 |
| C、X:氢氧化钡溶液Y:二氧化碳 |
| D、X:偏铝酸钠溶液Y:二氧化氮 |
取一定质量的均匀固体混合物Cu、Cu2O和 CuO,将其分成两等份,取其中一份用足量的氢气还原,测得反应后固体质量减少6.40g,另一份中加入500mL稀硝酸,固体恰好完全溶解,且同时收集到标准状况下NO气体4.48L,则所用硝酸的物质的量浓度为( )
| A、3.6mol/L |
| B、3.2mol/L |
| C、2.8mol/L |
| D、2.4mol/L |
下列说法中不正确的是( )
| A、不需要加热就能发生的发应一定是放热反应 |
| B、吸热反应在常温下可能发生 |
| C、反应吸热还是放热,取决于反应物和生成物所具有的总能量的相对大小 |
| D、物质发生化学变化一定伴随着能量变化 |
 ,物质A在体内脱氢酶的作用下会氧化为有害物质GHB.下图是关于物质A的一种制备方法及由A引发的一系列化学反应.
,物质A在体内脱氢酶的作用下会氧化为有害物质GHB.下图是关于物质A的一种制备方法及由A引发的一系列化学反应.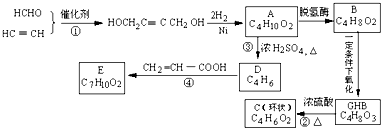
 结构),它的结构简式为
结构),它的结构简式为