0 131253 131261 131267 131271 131277 131279 131283 131289 131291 131297 131303 131307 131309 131313 131319 131321 131327 131331 131333 131337 131339 131343 131345 131347 131348 131349 131351 131352 131353 131355 131357 131361 131363 131367 131369 131373 131379 131381 131387 131391 131393 131397 131403 131409 131411 131417 131421 131423 131429 131433 131439 131447 203614



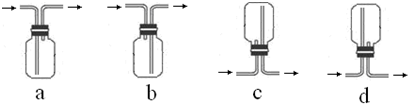
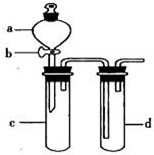 某兴趣小组设计出如图所示装置来改进教材中“铜与硝酸反应”实验,以探究化学实验的绿色化.
某兴趣小组设计出如图所示装置来改进教材中“铜与硝酸反应”实验,以探究化学实验的绿色化.
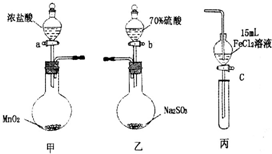 为验证氧化性
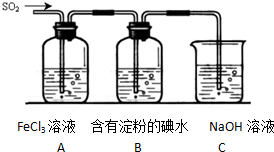
为验证氧化性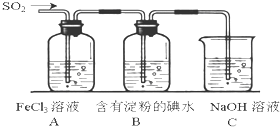 某校化学兴趣小组为探究SO2气体的还原性设计了如下装置图:
某校化学兴趣小组为探究SO2气体的还原性设计了如下装置图: