对于反应CO(g)+H2O(g)?CO2(g)+H2(g)△H<0,在其他条件不变的情况下,下列说法正确的是( )
| A、改变压强,平衡不发生移动,反应放出的热量不变 |
| B、若在原电池中进行,反应放出的热量不变 |
| C、升高温度,反应速率加快,反应放出的热量不变 |
| D、加入催化剂,改变了反应的途径,也改变了反应的△H |
下列物质属于电解质的是( )
| A、铜 |
| B、NaOH |
| C、蔗糖 |
| D、CO2 |
四种基本反应类型中,一定是氧化还原反应的是( )
| A、化合反应 | B、分解反应 |
| C、置换反应 | D、复分解反应 |
下列物质能导电,且为电解质的是( )
| A、蔗糖 |
| B、KNO3晶体 |
| C、盐酸 |
| D、熔化的NaCl |
工业制硫酸中的一步重要反应是SO2在400~500℃下的催化氧化:2SO2+O2
2SO3,这是一个正反应放热的可逆反应.如果反应在密闭容器中进行,下述有关说法中错误的是( )
| V2O5 |
| △ |
| A、使用催化剂是为了加快反应速率,提高生产效率 |
| B、在上述条件下,SO2不可能100%地转化为SO3 |
| C、为了提高SO2的转化率,应适当提高O2的浓度 |
| D、达到平衡时,SO2的浓度与SO3的浓度相等 |
25℃时,pH=5的NH4Cl溶液中,由水电离出的OH-浓度是( )
| A、1×10-5mol/L |
| B、1×10-7mol/L |
| C、1×10-9mol/L |
| D、1×10-14mol/L |
对于可逆反应N2(g)+3H2(g)?2NH3(g)△H<0,下列研究目的和示意图相符的是( )
| A | B | C | D | |
| 研究目的 | 压强对反应的影响(P2>P1) | 温度对反应的影响 | 平衡体系增加N2对反应的影响 | 催化剂对反应的影响 |
| 图示 | 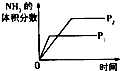 | 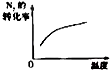 | 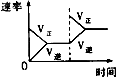 | 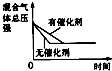 |
| A、A | B、B | C、C | D、D |
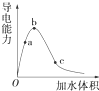 一定温度下,将一定质量的冰醋酸加水稀释过程中,溶液的导电能力变化如图所示.
一定温度下,将一定质量的冰醋酸加水稀释过程中,溶液的导电能力变化如图所示.