下列说法不正确的是( )
| A、焓变是与反应能否自发进行有关的因素,多数能自发进行的反应都是放热反应 |
| B、一个反应能否自发进行取决于该反应放热还是吸热 |
| C、在同一条件下不同物质有不同的熵值,其体系的混乱程度越大,熵值越大 |
| D、一个反应能否自发进行,与焓变和熵变的共同影响有关 |
下列关于热化学反应的描述中正确的是( )
| A、HCl和NaOH反应的中和热△H=-57.3 kJ/mol,则H2SO4和Ca(OH)2反应的中和热△H=2×(-57.3)kJ/mol |
| B、反应热是1mol物质参加反应时的能量变化 |
| C、需要加热才能发生的反应不一定是吸热反应 |
| D、1 mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热 |
下列说法中,正确的是( )
①同种元素的原子性质一定相同
②能自发进行的化学反应,不一定是△H<0、△S>0
③主族元素X、Y能形成XY2型化合物,则X与Y的原子序数之差可能为2或5
④Ksp不仅与难溶电解质的性质和温度有关,而且与溶液中的离子浓度有关
⑤“冰,水为之,而寒于水”说明相同质量的水和冰,水的能量高
⑥金属导电和电解质溶液的导电都是物理变化.
①同种元素的原子性质一定相同
②能自发进行的化学反应,不一定是△H<0、△S>0
③主族元素X、Y能形成XY2型化合物,则X与Y的原子序数之差可能为2或5
④Ksp不仅与难溶电解质的性质和温度有关,而且与溶液中的离子浓度有关
⑤“冰,水为之,而寒于水”说明相同质量的水和冰,水的能量高
⑥金属导电和电解质溶液的导电都是物理变化.
| A、①④⑥ | B、②③⑤ |
| C、②④⑤ | D、①③⑥ |
实验测得甲烷的燃烧热(△H=-890.3KJ/mol).则下列表示甲烷燃烧热的热化学方程式正确的是( )
| A、CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3KJ/mol | ||||
| B、CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890.3KJ/mol | ||||
C、
| ||||
D、
|
下列化学用语正确的是( )
| A、A乙醇的结构式:CH3CH2OH |
| B、乙烯的结构简式:C2H4 |
C、氯化钠的电子式: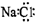 |
D、硫离子的结构示意图: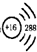 |
下列说法中,正确的是( )
| A、在化学反应过程中,发生物质变化的同时不一定发生能量变化 |
| B、反应产物的总焓大于反应物的总焓时,反应吸热,△H>0 |
| C、破坏生成物全部化学键所需要的能量大于破坏反应物全部化学键所需要的能量时,反应为吸热反应 |
| D、△H的大小与热化学方程式的计量数无关 |
下列文字表述与反应方程式对应且正确的是( )
| A、氯化铁溶液与铁单质反:Fe3++2Fe═3Fe2+ | ||
| B、用醋酸除去水垢:CaCO3+2H+═Ca2++H2O+CO2↑ | ||
| C、乙醇和钠反应:CH3CH2OH+Na→CH3CH2ONa+H2↑ | ||
D、实验室用液溴和苯在催化剂作用下制溴苯: +Br2 +Br2
 +HBr +HBr |
下列说法正确的是( )
| A、甲烷的标准燃烧热为890.3KJ?mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-890.3KJ?mol-1 | |||
B、500°C,30MPa下,将0.5molN2和1.5H2置于密闭的容器中充分反应生成NH3(g),放热19.3KJ,其热化学方程式为:N2(g)+3H2(g)
| |||
| C、常温下,反应C(s)+CO2(g)=2CO(g)不能自发进行,则该反应的△H>0 | |||
| D、同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件的△H不同 |
下列说法不正确的是( )
| A、用电解法精炼粗铜时纯铜作阳极 |
| B、FeCI3、CuSO4溶液均能使H2O2的分解速率加快 |
| C、常温下,0.1mol/LCH3COONa溶液pH大于7 |
| D、炒过菜地铁锅未及时洗净被锈蚀,正极反应式为O2+2H2O+4e-═4OH- |